Hvorfor er lys en vigtig faktor i alle kemiske reaktioner?
Her er hvorfor:
* Ikke alle reaktioner involverer lysabsorption: Mange kemiske reaktioner forekommer gennem kollisioner mellem molekyler, drevet af faktorer som temperatur, koncentration og katalysatorer. Lys er ikke involveret i disse processer.
* Lysenergi er ikke altid tilstrækkelig: Den energi, der kræves for at bryde kemiske bindinger og drive en reaktion, varierer meget. Mens lys i nogle tilfælde kan give energi, er dets energiniveau ofte utilstrækkeligt til at indlede reaktioner.
Lys spiller imidlertid en afgørende rolle i nogle specifikke typer reaktioner:
* fotokemiske reaktioner: Disse reaktioner initieres direkte af absorptionen af lysenergi, der begejstrer elektroner i molekyler og fører til bindingsbrud eller dannelse. Eksempler inkluderer fotosyntese, fotolyse og dannelse af ozon.
* fotokatalyse: Visse materialer, kendt som fotokatalysatorer, bruger lysenergi til at lette kemiske reaktioner. De absorberer lys, ophidser elektroner og skaber reaktive arter, der kan fremme kemiske transformationer.
* spektroskopi: Lys bruges til at analysere strukturen og egenskaberne af molekyler, der giver information om deres kemiske sammensætning og reaktioner.
Kortfattet:
Lys er en vigtig faktor i specifikke typer kemiske reaktioner , hovedsageligt dem, der involverer den direkte absorption af lysenergi. Det er dog ikke en universel faktor for alle kemiske reaktioner. Mange reaktioner fortsætter uden nogen indflydelse fra lys.
 Varme artikler
Varme artikler
-
 Analytiske metoder hjælper med at udvikle modgift mod cyanid, sennepsgasProfessor Brian Logue, venstre, ser som postdoktoral forskningsassistent Erica Manandhar pipetterer blod i centrifugerør. Kredit:South Dakota State University For at udvikle modgift mod kemiske mi
Analytiske metoder hjælper med at udvikle modgift mod cyanid, sennepsgasProfessor Brian Logue, venstre, ser som postdoktoral forskningsassistent Erica Manandhar pipetterer blod i centrifugerør. Kredit:South Dakota State University For at udvikle modgift mod kemiske mi -
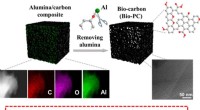 Grænseflade-induceret fremstilling af porøst kulstof med forbedrede iboende aktive stederUnder ikke-oxidationsbetingelser blev in-situ dannet aluminiumoxid/carbon-grænseflade udviklet som en vugge til generering af tilgængelige aktive steder. Det kan også justere den porøse struktur af re
Grænseflade-induceret fremstilling af porøst kulstof med forbedrede iboende aktive stederUnder ikke-oxidationsbetingelser blev in-situ dannet aluminiumoxid/carbon-grænseflade udviklet som en vugge til generering af tilgængelige aktive steder. Det kan også justere den porøse struktur af re -
 Retsmedicinsk analysemetode for læbestiftsspor udvikletKredit:Unsplash/CC0 Public Domain Retsmedicinere finder en ny måde at identificere mærker af læbestift på et gerningssted uden at fjerne beviser fra tasken. Ved hjælp af en teknik kaldet Raman -s
Retsmedicinsk analysemetode for læbestiftsspor udvikletKredit:Unsplash/CC0 Public Domain Retsmedicinere finder en ny måde at identificere mærker af læbestift på et gerningssted uden at fjerne beviser fra tasken. Ved hjælp af en teknik kaldet Raman -s -
 Ny teknik til bestemmelse af afstand i cellerIn-celleafstandsbestemmelse ved EPR afslører væsentlig strukturel information om biomakromolekyler under native betingelser. For første gang, den pulserede EPR -teknik RIDME (relaxation induced dipola
Ny teknik til bestemmelse af afstand i cellerIn-celleafstandsbestemmelse ved EPR afslører væsentlig strukturel information om biomakromolekyler under native betingelser. For første gang, den pulserede EPR -teknik RIDME (relaxation induced dipola
- Hvad er uranus beskrivelse?
- Langsomhedens afkodning:Zoologer finder ud af, hvordan dovendyr perfektionerede energibesparelser
- Hvordan hjalp F-skalaen forsker med at lære mere om uforudsigelige tornadoer?
- Fire ting, australske skoler bør gøre nu for at hjælpe med at forhindre kønsbaseret vold
- Erosionseffekter på økosystem
- Får friktion genstande til at bevæge sig hurtigere eller flyve højere?


