Er der en bevarelse af masse under kemisk reaktion?
Her er hvorfor:
* atomer oprettes ikke eller ødelægges: Kemiske reaktioner involverer omarrangement af atomer, ikke oprettelse eller ødelæggelse af dem. Atomerne, der findes i reaktanterne, omorganiseres simpelthen for at danne nye produkter.
* masse er en egenskab ved stof: Massen af et stof bestemmes af antallet af atomer, det indeholder. Da antallet af atomer forbliver konstant, skal den samlede masse også forblive konstant.
Eksempel:
Overvej reaktionen af brintgas (H2) med iltgas (O2) til dannelse af vand (H2O):
2H2 + O2 → 2H2O
* reaktanter: 2 molekyler af H2 (4 hydrogenatomer) og 1 molekyle O2 (2 iltatomer)
* Produkter: 2 molekyler af H2O (4 hydrogenatomer og 2 iltatomer)
Bemærk, at antallet af atomer i hvert element er det samme på begge sider af ligningen. Derfor svarer den samlede masse af reaktanterne den samlede masse af produkterne.
Vigtig note:
* Loven om bevarelse af masse gælder for lukkede systemer, hvilket betyder, at uanset kan komme ind eller forlade.
* Nukleare reaktioner, der involverer ændringer i kernen i et atom, er en undtagelse fra denne lov. I disse reaktioner kan en vis masse konverteres til energi og omvendt, som beskrevet af Einsteins berømte ligning E =MC².
 Varme artikler
Varme artikler
-
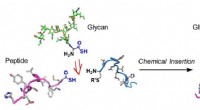 En vindende kombination til glykoproteinsynteseGlycoproteinsyntese ved kemisk indsættelse ved hjælp af en thiosyremedieret strategi:Metoden samler et fuldt glycoproteinsegment i to trin. Kredit:Osaka University Mange processer i kroppen regule
En vindende kombination til glykoproteinsynteseGlycoproteinsyntese ved kemisk indsættelse ved hjælp af en thiosyremedieret strategi:Metoden samler et fuldt glycoproteinsegment i to trin. Kredit:Osaka University Mange processer i kroppen regule -
 Ny metode til at løse plastiks bæredygtighedsproblemDr. Junpeng Wang. Kredit:University of Akron Bæredygtighed i plast er kommet langt i de seneste år, i høj grad takket være videnskabelige fremskridt. Men selvom plast bliver mere og mere miljøvenl
Ny metode til at løse plastiks bæredygtighedsproblemDr. Junpeng Wang. Kredit:University of Akron Bæredygtighed i plast er kommet langt i de seneste år, i høj grad takket være videnskabelige fremskridt. Men selvom plast bliver mere og mere miljøvenl -
 Polymerbevægelse:nøglen til næste generation af belægningerKredit:Texas A&M University Forskere ved Institut for Materialevidenskab og Teknik ved Texas A&M University, ledet af ph.d.-studerende Victor Selin og Dr. Svetlana Sukhishvili, gør fremskridt med
Polymerbevægelse:nøglen til næste generation af belægningerKredit:Texas A&M University Forskere ved Institut for Materialevidenskab og Teknik ved Texas A&M University, ledet af ph.d.-studerende Victor Selin og Dr. Svetlana Sukhishvili, gør fremskridt med -
 En ny cermet, der kunne give en bedre varmeudveksling til solenergianlægEn nylig udvikling ville gøre elproduktion fra solens varme mere effektiv, ved at bruge keramiske metalplader til varmeoverførsel ved højere temperaturer og ved forhøjede tryk. Kredit:Purdue Universit
En ny cermet, der kunne give en bedre varmeudveksling til solenergianlægEn nylig udvikling ville gøre elproduktion fra solens varme mere effektiv, ved at bruge keramiske metalplader til varmeoverførsel ved højere temperaturer og ved forhøjede tryk. Kredit:Purdue Universit
- Hvad er energi produceret af varmen inden for Jorden?
- Sensor måler yoctonewton-kræfter hurtigt
- Hvor er bromet i det periodiske system?
- Hvad er et eksempel på konvergent udvikling i tundraen?
- Tyskland planlægger at forbyde engangsplastikposer næste år
- Belle II giver de første resultater:På jagt efter Z ′ bosonen


