Hvad er arten af P O -binding i phosphorpentoxid P2O5?
* Elektronegativitetsforskel: Oxygen er mere elektronegativ end fosfor. Dette betyder, at ilt har en stærkere tiltrækning for de delte elektroner i bindingen, hvilket fører til en delvis negativ ladning (Δ-) på iltatomet og en delvis positiv ladning (Δ+) på phosphoratomet.
* ionisk karakter: Den store elektronegativitetsforskel mellem fosfor og ilt bidrager til en signifikant ionisk karakter i P-O-bindingen. Dette betyder, at elektronerne i bindingen ikke deles ens, men er tættere forbundet med iltatomet.
* polær kovalent binding: Mens den ioniske karakter er betydelig, involverer P-O-bindingen stadig deling af elektroner, hvilket gør den til en polær kovalent binding.
Struktur af P₂O₅:
P₂O₅ findes i forskellige former, men den mest almindelige er tetrahedral P₄O₁₀ . Dette molekyle består af fire fosforatomer, der hver er bundet til fire iltatomer i et tetrahedralt arrangement. Oxygenatomerne er arrangeret på en måde, der skaber to typer P-O-bindinger:
* p =o: Dette er dobbeltobligationer og er kortere og stærkere end P-O-enkeltbindingerne.
* p-o-p: Dette er enkeltbindinger, der forbinder fosforatomerne.
Vigtig note: Den signifikante ioniske karakter i P-O-bindingen bidrager til den stærkt reaktive karakter af phosphorpentoxid. Det reagerer let med vand til dannelse af fosforsyre (H₃po₄), en stærk syre.
Sidste artikelHvilke molekyler indeholder flere kulstofringe?
Næste artikelHvad sker der med natriummetal, når det udsættes for luft?
 Varme artikler
Varme artikler
-
 Forskere demonstrerer nye måder at opnå selektivitet for biomarkører inden for bioelektronikErin Ratcliff, venstre, og bachelorstuderende Zachary Kushlan undersøger en organisk halvleder tynd film fremstillet i Ratcliff -laboratoriet. Kredit:University of Arizona Ingeniører ved Universit
Forskere demonstrerer nye måder at opnå selektivitet for biomarkører inden for bioelektronikErin Ratcliff, venstre, og bachelorstuderende Zachary Kushlan undersøger en organisk halvleder tynd film fremstillet i Ratcliff -laboratoriet. Kredit:University of Arizona Ingeniører ved Universit -
 Nye stoffer med antivirale egenskaberKredit:CC0 Public Domain Brasilianske tekstilvirksomheder er begyndt at producere og markedsføre stoffer behandlet med sølv- og silica -nanopartikler udviklet af forskningsgrupperne ved Center for
Nye stoffer med antivirale egenskaberKredit:CC0 Public Domain Brasilianske tekstilvirksomheder er begyndt at producere og markedsføre stoffer behandlet med sølv- og silica -nanopartikler udviklet af forskningsgrupperne ved Center for -
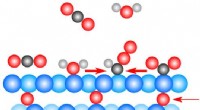 Forskere finder en overraskelse lige under overfladen i kuldioxideksperimentI denne illustration på atomare skala, spormængder af ilt (rød) lige under en kobber (blå) overflade, spiller en nøglerolle i at drive en katalytisk reaktion, hvor kuldioxid (sorte og røde molekyler)
Forskere finder en overraskelse lige under overfladen i kuldioxideksperimentI denne illustration på atomare skala, spormængder af ilt (rød) lige under en kobber (blå) overflade, spiller en nøglerolle i at drive en katalytisk reaktion, hvor kuldioxid (sorte og røde molekyler) -
 Neurovidenskabsmænd opdager ny struktur af vigtigt protein i hjernenAnimation af LeuT-transporterens fire trin sat sammen til en fuld cyklus. Kredit:Københavns Universitet Efter fem års eksperimenter, Det er lykkedes forskere fra Københavns Universitet at udkrysta
Neurovidenskabsmænd opdager ny struktur af vigtigt protein i hjernenAnimation af LeuT-transporterens fire trin sat sammen til en fuld cyklus. Kredit:Københavns Universitet Efter fem års eksperimenter, Det er lykkedes forskere fra Københavns Universitet at udkrysta
- At studere virale udbrud i enkeltceller kan afsløre nye måder at besejre dem på
- Dværgstjerne 200 lysår væk indeholder livets byggesten
- Hvad er den mængde varme, der kræves for at hæve temperaturen et stof gennem ti graders celsius?
- Hvordan vil erosion og aflejring påvirke en bjergkæde?
- Hvorfor er North Star lyseste på nattehimlen?
- Sådan beregnes firkantede fødder fra omkredsen


