Beregn massen af fast stof, der er nødvendigt for at fremstille opløsning 100 ml, der er 1,0 m i natriumkation ved hjælp af chlorid?
1. Bestem formlen for chloridsalt
Da vi ønsker en 1,0 m opløsning af natriumkationer (Na+), er chloridsaltet, vi bruger, natriumchlorid (NaCl) .
2. Beregn den molære masse af NaCl
* NA:22,99 g/mol
* Cl:35,45 g/mol
* Molmasse NaCl =22.99 + 35.45 =58.44 g/mol
3. Beregn molen for NaCl nødvendigt
* Molaritet (m) =mol opløst / liter opløsning
* Vi ønsker en 1,0 m opløsning og 100 ml (0,1 l) opløsning.
* mol NaCl =molaritet x volumen =1,0 m x 0,1 l =0,1 mol
4. Beregn massen af NaCl nødvendigt
* masse =mol x molmasse
* Masse =0,1 mol x 58,44 g/mol =5,844 g
Derfor har du brug for 5,844 gram natriumchlorid (NaCl) for at fremstille en 100 ml opløsning, der er 1,0 m i natriumkation.
 Varme artikler
Varme artikler
-
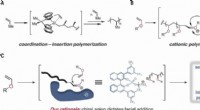 Brug af en organokatalysator til at stereokontrollere polymerisationDesign af en stereoselektiv kationisk polymerisation. (A) Det chirale ligandmiljø i koordinations-insertion-polymerisationer muliggør stereoselektiv monomer-enchainment ved at dirigere ansigtsaddition
Brug af en organokatalysator til at stereokontrollere polymerisationDesign af en stereoselektiv kationisk polymerisation. (A) Det chirale ligandmiljø i koordinations-insertion-polymerisationer muliggør stereoselektiv monomer-enchainment ved at dirigere ansigtsaddition -
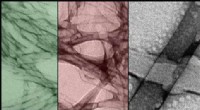 Formskiftende materialer:Brug af lys til at omarrangere makroskopiske strukturerTEM-billeder af selvsamlende nanostrukturer og deres rekombinationer, i falske farver. Kredit:Okinawa Institute of Science and Technology Graduate University - OIST OIST-forskere skaber selvsamlen
Formskiftende materialer:Brug af lys til at omarrangere makroskopiske strukturerTEM-billeder af selvsamlende nanostrukturer og deres rekombinationer, i falske farver. Kredit:Okinawa Institute of Science and Technology Graduate University - OIST OIST-forskere skaber selvsamlen -
 Benchmarks for bedre at fange solenYuliar Firdaus og kolleger har udviklet en beregningsmetode til at forudsige effektivitetsgrænser og foreslå designregler for ikke-fulleren organiske solceller. Kredit:King Abdullah University of Scie
Benchmarks for bedre at fange solenYuliar Firdaus og kolleger har udviklet en beregningsmetode til at forudsige effektivitetsgrænser og foreslå designregler for ikke-fulleren organiske solceller. Kredit:King Abdullah University of Scie -
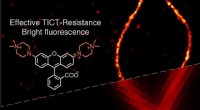 Oplyser vejen til superopløsningsbilleddannelse med forbedrede rhodaminfarvestofferForskere fra DUT og SUTD udviklede en ny klasse af kvaternære piperazin-substituerede rhodaminer med fremragende kvanteudbytter (Φ =0,93) og overlegen lysstyrke (ε × Φ =8,1 × 104 L·mol-1·cm-1), til bi
Oplyser vejen til superopløsningsbilleddannelse med forbedrede rhodaminfarvestofferForskere fra DUT og SUTD udviklede en ny klasse af kvaternære piperazin-substituerede rhodaminer med fremragende kvanteudbytter (Φ =0,93) og overlegen lysstyrke (ε × Φ =8,1 × 104 L·mol-1·cm-1), til bi
- Hvad hedder den virkning, der viser, at nogle stjerner er tættere end os andre?
- Hvilken sedimentær bjergart ville blive dannet ved komprimering og cementering af partikler på 1,5…
- Etablering af oprindelsen til solmasser sorte huller og forbindelsen til mørkt stof
- Hvordan konverterer jeg målingen 0,005 gram til videnskabelig notation?
- Hvorfor det betaler sig offline at turde sammenligne onlinepriser
- Er et meget brændbart stof også et reaktivt stof?


