Hvorfor ikke vandig opløsning af natriumchlorid anvendt i stedet smeltet?
* vand er fortrinsvis elektrolyseret: Når du anvender elektricitet på en vandig opløsning af natriumchlorid, er vandmolekyler lettere elektrolyseret end chloridionerne. Dette fører til dannelse af brintgas ved katoden og iltgas ved anoden snarere end natrium og klor.
* sikkerhedsmæssige bekymringer: Elektrolyserende vand i en vandig opløsning af natriumchlorid producerer brint- og klorgasser. Hydrogen er brandfarligt, og klor er giftigt, hvilket gør denne proces meget farlig.
Hvorfor smeltet natriumchlorid bruges i stedet:
* Ingen vandinterferens: Ved at bruge smeltet natriumchlorid (NaCl) eliminerer du vand fra systemet og forhindrer, at det er elektrolyseret. Dette tillader, at chloridionerne er elektrolyseret, hvilket producerer klorgas ved anoden.
* Direkte metalproduktion: Natriumionerne reduceres også ved katoden og producerer flydende natriummetal.
Kortfattet: Brug af smeltet natriumchlorid til elektrolyse sikrer:
* Direkte produktion af natriummetal og klorgas.
* Sikkerhed på grund af fraværet af brandfarlige og giftige gasser.
Denne proces er kendt som downs -processen , og det er den primære industrielle metode til produktion af natriummetal.
 Varme artikler
Varme artikler
-
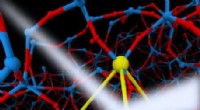 Hvad forårsager den top? Besvarelse af et langvarigt spørgsmål om kovalente væskerRøntgenspredning (hvid beem) billede af lokal tetraedrisk orden dannet af Si-atomer (store gule partikler) i flydende silica (Si-atomer er store partikler og O-atomer er små partikler) ved simulering.
Hvad forårsager den top? Besvarelse af et langvarigt spørgsmål om kovalente væskerRøntgenspredning (hvid beem) billede af lokal tetraedrisk orden dannet af Si-atomer (store gule partikler) i flydende silica (Si-atomer er store partikler og O-atomer er små partikler) ved simulering. -
 Kæmpe flexoelektricitetsgennembrud i bløde elastomerer baner vej for forbedrede robotter og selvdr…Kredit:CC0 Public Domain Forskere har demonstreret gigantisk flexoelektricitet i bløde elastomerer, der kan forbedre robottens bevægelsesområde og gøre selvdrevne pacemakere til en reel mulighed.
Kæmpe flexoelektricitetsgennembrud i bløde elastomerer baner vej for forbedrede robotter og selvdr…Kredit:CC0 Public Domain Forskere har demonstreret gigantisk flexoelektricitet i bløde elastomerer, der kan forbedre robottens bevægelsesområde og gøre selvdrevne pacemakere til en reel mulighed. -
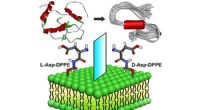 Nye fund kaster lys over udviklingen af liposom-baserede hæmmereMolekylær chiralitet medieret amyloiddannelse på phospholipidoverflader. Kredit:WANG Xue Alzheimers sygdom (AD) er en af de største globale folkesundhedsudfordringer. Imidlertid, patogenesen af
Nye fund kaster lys over udviklingen af liposom-baserede hæmmereMolekylær chiralitet medieret amyloiddannelse på phospholipidoverflader. Kredit:WANG Xue Alzheimers sygdom (AD) er en af de største globale folkesundhedsudfordringer. Imidlertid, patogenesen af -
 Bare bland det sammen:Ny syntetisk metode til fremstilling af amfifile molekyler uden tilsætningsst…Kredit:Dr. Masahiro Yamashina amfifile molekyler, som samler og indkapsler molekyler i vand, finde anvendelse inden for flere felter af kemi. Det enkle, additiv-fri forbindelse af hydrofile og hyd
Bare bland det sammen:Ny syntetisk metode til fremstilling af amfifile molekyler uden tilsætningsst…Kredit:Dr. Masahiro Yamashina amfifile molekyler, som samler og indkapsler molekyler i vand, finde anvendelse inden for flere felter af kemi. Det enkle, additiv-fri forbindelse af hydrofile og hyd
- Hvorfor er helixen så populær en form?
- Nye datingteknikker afslører Australiens ældste kendte klippemaleri, og det er en kænguru
- E. coli:Den ideelle transport til næste generations vacciner?
- Er forbrænding af kul en årsagssyreudfældning?
- Hvor mange atomer er der i C6H4Cl2?
- Elektroniske oscillationer i grafen kunne gøre en bordpladekilde til røntgenstråler til virkeligh…


