Hvad er produkterne fra ilt og svovl?
1. Svovldioxid (SO2):
* Dette er det mest almindelige produkt af reaktionen mellem ilt og svovl, især når svovl brændes i luften.
* Reaktionen er: S + O2 → SO2
* Svovldioxid er en farveløs gas med en skarp lugt. Det er et stort luftforurenende stof og bruges også til produktion af svovlsyre.
2. Svovltrioxid (SO3):
* Dette dannes, når svovldioxid reagerer yderligere med ilt: 2SO2 + O2 → 2SO3
* Svovltrioxid er en farveløs væske, der let opløses i vand til dannelse af svovlsyre.
3. Andre oxider:
* Afhængig af forholdene kan svovl også danne andre oxider som svovlmonoxid (SO), disulfurdioxid (S2O2) og disulfurmonoxid (S2O). Disse er mindre almindelige end svovldioxid og svovltrioxid.
4. Svovlsyre (H2SO4):
* Dette er ikke et direkte produkt af reaktionen mellem ilt og svovl, men det dannes, når svovltrioxid opløses i vand: SO3 + H2O → H2SO4
* Svovlsyre er en stærk syre og er en af de vigtigste industrikemikalier.
Det er vigtigt at bemærke, at reaktionen mellem ilt og svovl er eksoterm, hvilket betyder, at den frigiver varme. Dette kan observeres, når svovl brændes og producerer en lyse blå flamme.
Så produkterne fra ilt og svovl varierer afhængigt af de specifikke reaktionsbetingelser.
Sidste artikelHvorfor får halogener elektroner?
Næste artikelHvor mange stoffer er faste stoffer ved 0 grader Kelvin?
 Varme artikler
Varme artikler
-
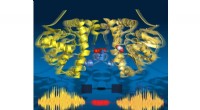 En molekylær strengtelefon på arbejdeTime-lapse-billeder viser, at enzymet ånder under omsætning:det udvider sig og trækker sig sammen i overensstemmelse med de katalytiske undertrin. Dens to halvdele kommunikerer via en række vandmoleky
En molekylær strengtelefon på arbejdeTime-lapse-billeder viser, at enzymet ånder under omsætning:det udvider sig og trækker sig sammen i overensstemmelse med de katalytiske undertrin. Dens to halvdele kommunikerer via en række vandmoleky -
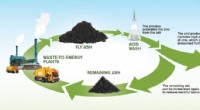 Udvinding af ædle zink fra affaldsaskeEn illustration af processen til genvinding af zink. Kredit:Yen Strandqvist/Chalmers Tekniske Universitet Forbrænding af fast affald producerer årligt millioner af tons affald flyveaske i Europa;
Udvinding af ædle zink fra affaldsaskeEn illustration af processen til genvinding af zink. Kredit:Yen Strandqvist/Chalmers Tekniske Universitet Forbrænding af fast affald producerer årligt millioner af tons affald flyveaske i Europa; -
 Plantebaserede og genanvendelige plastikflasker med citrusskal som råmaterialeKredit:Pixabay/CC0 Public Domain Skiftet fra fossilbaseret til vedvarende bioplast kræver nye effektive metoder. Ny teknologi udviklet på VTT muliggør brugen af pektinholdigt landbrugsaffald, så
Plantebaserede og genanvendelige plastikflasker med citrusskal som råmaterialeKredit:Pixabay/CC0 Public Domain Skiftet fra fossilbaseret til vedvarende bioplast kræver nye effektive metoder. Ny teknologi udviklet på VTT muliggør brugen af pektinholdigt landbrugsaffald, så -
 Forskere afdækker skjulte deicer -risici, der påvirker broens sundhedXianming Shi. Kredit:WSU Almindelige magnesiumchlorid tømidler, der bruges på veje og broer rundt om i USA, kan gøre mere skade end tidligere antaget, forskere har fundet. Derudover at skade er u
Forskere afdækker skjulte deicer -risici, der påvirker broens sundhedXianming Shi. Kredit:WSU Almindelige magnesiumchlorid tømidler, der bruges på veje og broer rundt om i USA, kan gøre mere skade end tidligere antaget, forskere har fundet. Derudover at skade er u


