Hvorfor danner helium ikke forbindelser?
* Fuld valence Shell: Helium har en fyldt 1S -orbital, der indeholder to elektroner. Dette gør det utroligt stabilt, da det tilfredsstiller oktetreglen og ikke har noget "ønske" at vinde eller miste elektroner.
* Høj ioniseringsenergi: Det kræver en enorm mængde energi for at fjerne et elektron fra Heliums stabile konfiguration. Dette gør det meget vanskeligt at danne kationer (positivt ladede ioner).
* lille atomstørrelse: Heliums lille størrelse fører til en stærk attraktion mellem dens kerne og elektroner, hvilket yderligere øger dens stabilitet.
* Mangel på tomme orbitaler: Helium mangler tomme orbitaler for at rumme elektroner fra andre atomer. Dette gør det ekstremt vanskeligt at danne kovalente bindinger (deling af elektroner).
Undtagelser:
Mens helium generelt betragtes som ureaktiv, er der nogle meget sjældne og eksotiske undtagelser, som dannelsen af:
* heliumhydridion (heh+) :Dette er en meget ustabil art, der kun observeres under ekstremt barske forhold som det interstellære medium.
Kortfattet: Heliums ekstraordinære stabilitet på grund af dens fulde valensskal, høj ioniseringsenergi, lille størrelse og mangel på tomme orbitaler gør det ekstremt modstandsdygtigt over for dannelse af forbindelser. Det er en ædel gas, indhold i sin egen tilstand og generelt glad for bare at eksistere.
 Varme artikler
Varme artikler
-
 Gennembrud skabt ved påvisning af kulstof -urenheder i galliumnitridkrystaller via lysGaN-krystaller under foto-excitation. Kulstofkoncentration fra venstre mod højre:høj, medium, og lav. Kredit:Kazunobu Kojima Kulstofrenhed har længe hindret effektiviteten i nitridbaserede elektro
Gennembrud skabt ved påvisning af kulstof -urenheder i galliumnitridkrystaller via lysGaN-krystaller under foto-excitation. Kulstofkoncentration fra venstre mod højre:høj, medium, og lav. Kredit:Kazunobu Kojima Kulstofrenhed har længe hindret effektiviteten i nitridbaserede elektro -
 Direkte elektrolyse har blandede resultater for udvinding af brændstofkilder fra mikroalgerForskere undersøger måder at forbedre lipidekstraktion fra mikroalger til fremstilling af biobrændstoffer. Kredit:123rf/Akhararat Wathanasing Forskere undersøger måder at forbedre produktionen af
Direkte elektrolyse har blandede resultater for udvinding af brændstofkilder fra mikroalgerForskere undersøger måder at forbedre lipidekstraktion fra mikroalger til fremstilling af biobrændstoffer. Kredit:123rf/Akhararat Wathanasing Forskere undersøger måder at forbedre produktionen af -
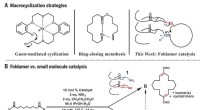 Efterligner enzymer, kemikere producerer store, nyttige carbonringeMakrocykliseringsstrategier. (A) Tidligere tilgange og foldamertilgang til makrocyklisering. (B) Divergent reaktivitet:Foldamer versus små molekyle katalyse. lign., ækvivalent(er). Kredit: Videnskab
Efterligner enzymer, kemikere producerer store, nyttige carbonringeMakrocykliseringsstrategier. (A) Tidligere tilgange og foldamertilgang til makrocyklisering. (B) Divergent reaktivitet:Foldamer versus små molekyle katalyse. lign., ækvivalent(er). Kredit: Videnskab -
 Udvideligt skum til 3D-udskrivning af store objekterKredit:CC0 Public Domain Det er en frustrerende begrænsning ved 3D-print:Udskrevne objekter skal være mindre end den maskine, der fremstiller dem. Kæmpe maskiner er upraktiske til at printe store
Udvideligt skum til 3D-udskrivning af store objekterKredit:CC0 Public Domain Det er en frustrerende begrænsning ved 3D-print:Udskrevne objekter skal være mindre end den maskine, der fremstiller dem. Kæmpe maskiner er upraktiske til at printe store
- Den første observation af den nukleare Barnett-effekt
- Undersøgelse dokumenterer den første menneskelige besættelse i Nordafrika
- Forbedret mid-infrarød nanoskopi giver 30 gange klarere udsyn til bakteriernes indre
- Hvordan stemmer du imod sommertid?
- Firefly-gen belyser evnen hos optimeret CRISPR-Cpf1 til effektivt at redigere menneskeligt genom
- Hvordan kan du bestemme eksperimentelt, om et stof er til stede i ionisk molekylær form eller ej, n…


