Hvordan gælder loven om bevaringsmassen for kemiske reaktioner?
1. Atomer oprettes hverken eller ødelægges:
* Kemiske reaktioner involverer omarrangement af atomer, ikke deres skabelse eller ødelæggelse.
* Atomerne, der er til stede i reaktanterne, omarrangeres simpelthen for at danne nye molekyler, produkterne.
2. Massen konserveres:
* Da antallet og typer atomer forbliver de samme, forbliver den samlede masse af systemet også den samme.
* Ingen masse går tabt eller opnås under en kemisk reaktion.
Eksempel:
Overvej reaktionen af brintgas (H₂) med iltgas (O₂) til dannelse af vand (H₂O):
2H₂ + O₂ → 2H₂O
* reaktanter: 4 hydrogenatomer og 2 iltatomer.
* Produkter: 4 hydrogenatomer og 2 iltatomer.
Antallet og typer af atomer er de samme på begge sider af ligningen, så den samlede masse bevares.
implikationer:
* afbalancering af kemiske ligninger: Loven om bevarelse af masse er afgørende for at afbalancere kemiske ligninger, hvilket sikrer, at det samme antal af hver type atom vises på begge sider.
* støkiometri: At forstå bevarelsen af masse giver os mulighed for at beregne mængden af reaktanter og produkter, der er involveret i en reaktion, baseret på deres molære masser.
* Miljøapplikationer: Dette princip er vigtigt for at forstå miljøprocesser som forbrænding og forurening, hvor massen af de frigivne forurenende stoffer skal svare til massen af de originale materialer, der forbruges.
Vigtig note:
* Loven om bevarelse af masse gælder for lukkede systemer, hvor uanset kan du gå ind eller forlade.
* I åbne systemer kan masse synes at gå tabt på grund af faktorer som fordampning eller frigivelse af gasser.
* I nukleare reaktioner er loven om bevarelse af masse ikke strengt sandt, da en eller anden masse omdannes til energi. Imidlertid forbliver den samlede energi og masse konstant, som beskrevet af Einsteins berømte ligning, E =MC².
Generelt er loven om bevarelse af masse et grundlæggende princip i kemi og er vigtig for at forstå, hvordan kemiske reaktioner forekommer, og hvordan stof opfører sig.
 Varme artikler
Varme artikler
-
 Planetarisk kuglefræsning hjælper med at beskytte vores planet mod plastikforureningFunktioner af de supramolekylære materialer. Da materialerne blev såret, de helede inden for 1 min. Yderligere, når den påføres som belægning på et glasunderlag, materialet viste ekstremt hurtige helb
Planetarisk kuglefræsning hjælper med at beskytte vores planet mod plastikforureningFunktioner af de supramolekylære materialer. Da materialerne blev såret, de helede inden for 1 min. Yderligere, når den påføres som belægning på et glasunderlag, materialet viste ekstremt hurtige helb -
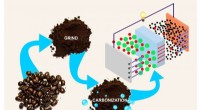 Kemikere syntetiserer elektroder til akkumulatorer fra kaffegrumsKredit:Natalia Deryugina En kemiker fra RUDN foreslog en billig og miljøvenlig måde at fremstille elektroder til lithium-ion-batterier fra kaffeproduktionsaffald. En artikel, der beskriver denne u
Kemikere syntetiserer elektroder til akkumulatorer fra kaffegrumsKredit:Natalia Deryugina En kemiker fra RUDN foreslog en billig og miljøvenlig måde at fremstille elektroder til lithium-ion-batterier fra kaffeproduktionsaffald. En artikel, der beskriver denne u -
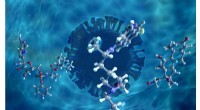 Neutroner undersøger molekylær adfærd hos foreslåede COVID-19 lægemiddelkandidaterBrug af neutroner, ORNL-forskere analyserede den molekylære dynamik i tidligere foreslåede COVID-19 lægemiddelkandidater remdesivir (til venstre), hydroxychlorokin (i midten), og dexamethason (til høj
Neutroner undersøger molekylær adfærd hos foreslåede COVID-19 lægemiddelkandidaterBrug af neutroner, ORNL-forskere analyserede den molekylære dynamik i tidligere foreslåede COVID-19 lægemiddelkandidater remdesivir (til venstre), hydroxychlorokin (i midten), og dexamethason (til høj -
 Smart label kunne en dag fortælle dig, hvornår du skal smide mad og kosmetikSmarte etiketter til kosmetik og fødevarer kunne en dag fortælle forbrugerne, hvornår de skal smide et produkt ud. Kredit:Silvana Andreescu Detektering af mad og kosmetisk fordærv og forurening. I
Smart label kunne en dag fortælle dig, hvornår du skal smide mad og kosmetikSmarte etiketter til kosmetik og fødevarer kunne en dag fortælle forbrugerne, hvornår de skal smide et produkt ud. Kredit:Silvana Andreescu Detektering af mad og kosmetisk fordærv og forurening. I
- Hvad betyder St. Thomas Aquinas, når han siger, at Grace bygger på naturen?
- Hvad er et eksempel på infest?
- Skyld ikke Dubais freak regn på skyfrø – stormen var alt for stor til at være menneskeskabt
- Verifikation af whisky ved hjælp af laserlys
- Sådan beregnes en spiral
- Video:Hvordan gamle iskerner viser 'sort svane' begivenheder i historien - selv pandemier


