Hvor mange nitrogenatomer er til stede i 5,00 g C2H5O2N?
1. Beregn den molære masse af C2H5O2N:
* C:2 atomer * 12,01 g/mol =24,02 g/mol
* H:5 atomer * 1,01 g/mol =5,05 g/mol
* O:2 atomer * 16,00 g/mol =32,00 g/mol
* N:1 atom * 14,01 g/mol =14,01 g/mol
Total molmasse på C2H5O2N =75,08 g/mol
2. Konverter gram af C2H5O2N til mol:
* mol =gram / molær masse
* mol =5,00 g / 75,08 g / mol
* mol ≈ 0,0666 mol
3. Beregn molen af nitrogenatomer:
* Da der er et nitrogenatom pr. Molekyle af C2H5O2N, er molen af nitrogen lig med molen på C2H5O2N:0,0666 mol
4. Konverter mol nitrogenatomer til antallet af atomer:
* Brug Avogadros nummer:6,022 x 10^23 atomer/mol
* Atomer af nitrogen =mol nitrogen * Avogadro's nummer
* Atomer af nitrogen =0,0666 mol * 6,022 x 10^23 atomer/mol
* Atomer af nitrogen ≈ 4,01 x 10^22 atomer
Derfor er der ca. 4,01 x 10^22 atomer af nitrogen, der er til stede i 5,00 g C2H5O2n.
 Varme artikler
Varme artikler
-
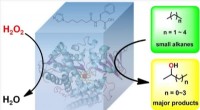 Forskere tager skridt mod mere effektive brændstofraffineringsprocesserKonstruktion af et enzym, der ensartet vil fremskynde de små alkaners reaktion på hydroxylgrupper, der er nødvendige for at producere brændstof. Kredit:CONG Zhiqi, Qingdao Institut for Bioenergi og Bi
Forskere tager skridt mod mere effektive brændstofraffineringsprocesserKonstruktion af et enzym, der ensartet vil fremskynde de små alkaners reaktion på hydroxylgrupper, der er nødvendige for at producere brændstof. Kredit:CONG Zhiqi, Qingdao Institut for Bioenergi og Bi -
 Forskere skaber holdbare, vaskbar tekstilbelægning, der kan afvise virusEn illustration viser det behandlede tekstils evne til at afvise væsker. Kredit:University of Pittsburgh Masker, kjoler, og andet personligt beskyttelsesudstyr (PPE) er afgørende for at beskytte s
Forskere skaber holdbare, vaskbar tekstilbelægning, der kan afvise virusEn illustration viser det behandlede tekstils evne til at afvise væsker. Kredit:University of Pittsburgh Masker, kjoler, og andet personligt beskyttelsesudstyr (PPE) er afgørende for at beskytte s -
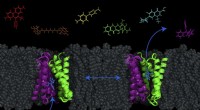 Ny model afslører muligheden for at pumpe antibiotika ind i bakterierEt transportørprotein - kaldet EmrE, vist i lilla og grønt -- i cellemembranen af E. coli kan bakterier skiftes mellem to konformationer for at pumpe molekyler (såsom antibakterielle lægemidler) ud
Ny model afslører muligheden for at pumpe antibiotika ind i bakterierEt transportørprotein - kaldet EmrE, vist i lilla og grønt -- i cellemembranen af E. coli kan bakterier skiftes mellem to konformationer for at pumpe molekyler (såsom antibakterielle lægemidler) ud -
 Den schweiziske hærkniv af røgskærmeEn ny type røggranat, der kan skjule sensorer i det synlige og infrarøde område, brænder under en test. Kredit:US Army At udløse røgbomber er mere end god fornøjelse den fjerde juli. Militæret bru
Den schweiziske hærkniv af røgskærmeEn ny type røggranat, der kan skjule sensorer i det synlige og infrarøde område, brænder under en test. Kredit:US Army At udløse røgbomber er mere end god fornøjelse den fjerde juli. Militæret bru
- Af hvilke faktorer, der vælger opløsningsmiddel, afhænger af?
- Hvorfor sammenlignes retningen af polarisationslys med vibrationselektroner, der producerede det?
- Hvad hedder en organisme, som kun dens producenter?
- NASA spejler på ESA pathfinder for at forbedre månenavigationen
- Nye bionedbrydelige polyurethanskum er udviklet af hvedestrå
- Hvordan søgen efter fodbolde er den næste store ting, giver næring til en moderne slavehandel


