Hvad er eksempler på amfoteriske oxider?
Eksempler på amfoteriske oxider:
Amfoteriske oxider er kemiske forbindelser, der kan fungere som både syrer og baser, afhængigt af det kemiske miljø. Her er nogle eksempler:
Almindelige eksempler:
* aluminiumoxid (al₂o₃): Reagerer med syrer til dannelse af salte og vand og med baser til dannelse af aluminater.
* zinkoxid (ZnO): Reagerer med syrer til dannelse af zinksalte og vand og med baser til dannelse af zinkater.
* bly (ii) oxid (PBO): Reagerer med syrer for at danne blysalte og vand og med baser til dannelse af VVS.
* tin (II) oxid (SNO): Reagerer med syrer for at danne tin salte og vand og med baser til dannelse af stannitter.
* chrom (III) oxid (cr₂o₃): Reagerer med syrer til dannelse af kromsalte og vand og med baser til dannelse af kromitter.
Mindre almindelige eksempler:
* berylliumoxid (BEO)
* galliumoxid (ga₂o₃)
* indiumoxid (in₂o₃)
* germaniumdioxid (geo₂) (undertiden klassificeret som sur)
Bemærk:
* Klassificeringen af et oxid som amfoterisk kan afhænge af de specifikke betingelser, såsom temperatur og koncentration.
* Nogle oxider, som sio₂ (siliciumdioxid) og P₄O₁₀ (phosphor pentoxid) , betragtes typisk surt, men kan udvise amfoterisk opførsel under visse betingelser.
reaktioner, der demonstrerer amfoterisk adfærd:
aluminiumoxid som syre:
Al₂o₃ + 6HCl → 2Alcl₃ + 3H₂O
aluminiumoxid som base:
Al₂o₃ + 2naOH + 3H₂O → 2NA [AL (OH) ₄]
Zinkoxid som syre:
ZnO + 2HCl → Zncl₂ + H₂O
Zinkoxid som base:
Zno + 2naOH + H₂O → NA₂ [Zn (OH) ₄]
Disse eksempler viser, at amfoteriske oxider kan reagere med både syrer og baser for at danne salte og vand. Denne unikke ejendom gør dem værdifulde i forskellige applikationer, herunder fremstilling, katalyse og pigmenter.
Sidste artikelEr hydrogenbromidpolar eller ikke -polær?
Næste artikelNavngiv et amfoterisk oxid reduceret af den grundlæggende gas?
 Varme artikler
Varme artikler
-
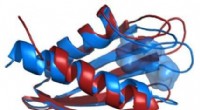 Røntgenøjne kigger dybere ind i dødbringende patogenSammenligning af strukturerne af Flpp3-proteinrygraden som afledt af en røntgenfri elektronlaser (rød) og fra NMR (blå) afslører et indre hulrum, der er unikt for NMR-strukturen og antyder derfor eksi
Røntgenøjne kigger dybere ind i dødbringende patogenSammenligning af strukturerne af Flpp3-proteinrygraden som afledt af en røntgenfri elektronlaser (rød) og fra NMR (blå) afslører et indre hulrum, der er unikt for NMR-strukturen og antyder derfor eksi -
 Vejskilte for immunforsvarscellerKredit:CC0 Public Domain Organismer bliver konstant invaderet af patogener såsom vira. Vores immunsystem går i gang for at bekæmpe disse patogener med det samme. Det medfødte uspecifikke immunrespo
Vejskilte for immunforsvarscellerKredit:CC0 Public Domain Organismer bliver konstant invaderet af patogener såsom vira. Vores immunsystem går i gang for at bekæmpe disse patogener med det samme. Det medfødte uspecifikke immunrespo -
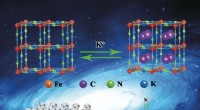 Direkte konvertering af rustent rustfrit stålnet til stabilt, billige elektroder til kalium-ion-bat…Kinesiske videnskabsmænd har gjort god brug af affald, mens de har fundet en innovativ løsning på et teknisk problem ved at omdanne rustent rustfrit stålnet til elektroder med fremragende elektrokemis
Direkte konvertering af rustent rustfrit stålnet til stabilt, billige elektroder til kalium-ion-bat…Kinesiske videnskabsmænd har gjort god brug af affald, mens de har fundet en innovativ løsning på et teknisk problem ved at omdanne rustent rustfrit stålnet til elektroder med fremragende elektrokemis -
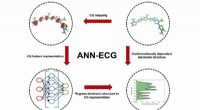 Ny tilgang til molekylær modellering kan fremskynde udviklingen af nye organiske materialer til e…Skematisk af ANN-EKG-metoden anvendt i dette arbejde. Skematisk eksempel viser en tre-perle/monomer grovkornet molekylær modelkortlægning for sexi (3-methyl) thiophen. Kredit:Argonne National Laborato
Ny tilgang til molekylær modellering kan fremskynde udviklingen af nye organiske materialer til e…Skematisk af ANN-EKG-metoden anvendt i dette arbejde. Skematisk eksempel viser en tre-perle/monomer grovkornet molekylær modelkortlægning for sexi (3-methyl) thiophen. Kredit:Argonne National Laborato
- Stoffet, der indeholder mange OH -ioner, er en?
- NASA-NOAAs Suomi NPP-satellit fanger tyfonen Yutu i styrkelse, Guam i alarmberedskab
- Ny teknologi fremmer beskyttelsen af kritiske systemer mod insiderstøttede angreb
- Er nitrogen en leder eller isolator af varme?
- Undersøgelse viser en grundlæggende forskel mellem, hvordan insekter, pattedyr opdager lugte
- Kan samarbejde mellem generationerne besejre klimaforandringerne?


