Forklar filmdannelsen i mælk, når natriumhydroxid tilsættes?
1. Naohs rolle:
* alkalinitet: NaOH er en stærk base, hvilket gør opløsningen meget alkalisk. Denne høje pH forstyrrer den delikate balance mellem ladninger inden for mælkeproteiner.
* ionstyrke: NaOH øger opløsningens ionstyrke, hvilket yderligere forstyrrer interaktionerne mellem proteinmolekyler.
2. Protein denaturering:
* Proteinstruktur: Mælkeproteiner som kasein- og valleproteiner har komplekse foldede strukturer, der holdes sammen af svage bindinger (brintbindinger, elektrostatiske interaktioner).
* Forstyrrelse af obligationer: Det alkaliske miljø og øget ionstyrke bryder disse svage bindinger, hvilket får proteinerne til at udfolde sig og miste deres oprindelige struktur (denaturering).
3. Koagulation:
* udsatte hydrofobe regioner: Når proteinerne udspiller sig, bliver hydrofobe regioner (vandafvisende) udsat. Disse regioner har en tendens til at klumpe sammen for at minimere kontakten med det omgivende vand.
* aggregering: De denaturerede proteiner aggregerer, der danner store klumper eller netværk. Denne aggregering fælder vand og andre komponenter i mælken og danner den observerede film.
4. Andre faktorer:
* Koncentration: Koncentrationen af NaOH påvirker i høj grad hastigheden og omfanget af koagulation. Højere koncentrationer fører til hurtigere og mere markant filmdannelse.
* Temperatur: Opvarmning fremskynder denaturerings- og koagulationsprocessen.
I resumé forstyrrer det tilsætning af natriumhydroxid til mælk strukturen af mælkeproteiner, hvilket får dem til at udfolde sig, aggregeres og danner en film. Denne proces er drevet af det alkaliske miljø og øget ionstyrke skabt af NaOH.
Bemærk: Denne reaktion ligner hvad der sker, når man laver ost. Tilsætningen af Rennet (et enzym) eller syrer som citronsaft får også mælkeproteiner til at koagulere og danne ostemasse.
 Varme artikler
Varme artikler
-
 Sensorer på planteblade advarer om vandmangelKunstnerens indtryk af sensoren bestående af ledende blæk trykt på tværs af en stomi med to mikrosøjler. Kredit:Betsy Skrip Har du glemt at vande den plante på dit skrivebord igen? Det kan snart v
Sensorer på planteblade advarer om vandmangelKunstnerens indtryk af sensoren bestående af ledende blæk trykt på tværs af en stomi med to mikrosøjler. Kredit:Betsy Skrip Har du glemt at vande den plante på dit skrivebord igen? Det kan snart v -
 Interaktion med nukleart affald i miljøet kan være mere kompliceret, end man engang troedeDen glødende/lyserøde prøve på højre side er en egentlig prøve, der indeholder radioaktivt curium og proteinet lanmodulin, under et fluorescensspektroskopiforsøg ved LLNL. Proteinet får curium til at
Interaktion med nukleart affald i miljøet kan være mere kompliceret, end man engang troedeDen glødende/lyserøde prøve på højre side er en egentlig prøve, der indeholder radioaktivt curium og proteinet lanmodulin, under et fluorescensspektroskopiforsøg ved LLNL. Proteinet får curium til at -
 DESYs røntgenkilde PETRA III afslører detaljer om klæbende strukturer af edderkoppebenFor at finde ud af, hvorfor jagtedderkoppen Cupiennius salei klæber så godt til lodrette overflader, det tværfaglige forskerhold undersøger de små klæbende hår på edderkoppebenene. Kredit:Universität
DESYs røntgenkilde PETRA III afslører detaljer om klæbende strukturer af edderkoppebenFor at finde ud af, hvorfor jagtedderkoppen Cupiennius salei klæber så godt til lodrette overflader, det tværfaglige forskerhold undersøger de små klæbende hår på edderkoppebenene. Kredit:Universität -
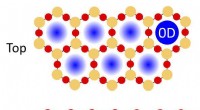 Dækning af metalkatalysatoroverflader med tynde todimensionale oxidmaterialer kan forbedre kemiske …En illustration af fysisk lukkede rum i en porøs dobbeltlags silica film på en metalkatalysator, der kan bruges til kemiske reaktioner. Siliciumatomer er angivet med de orange cirkler; iltatomer ved d
Dækning af metalkatalysatoroverflader med tynde todimensionale oxidmaterialer kan forbedre kemiske …En illustration af fysisk lukkede rum i en porøs dobbeltlags silica film på en metalkatalysator, der kan bruges til kemiske reaktioner. Siliciumatomer er angivet med de orange cirkler; iltatomer ved d
- Hvad gør lithiumcarbonat ved din krop?
- Video:Ildkugle set af vejrsatellit
- Hvordan planter kan vokse på saltpåvirket jord
- Forskere producerer nanodiamanter, der er i stand til at levere medicinske og kosmetiske midler genn…
- Hvordan anvendes valenselektroner af et atom til klassificering?
- Ændrer en plante sit look ved, hvor pollineret?


