Hvorfor er natriumhydroxid en stærk base?
* Komplet dissociation: Når NaOH opløses i vand, adskiller den sig fuldstændigt i dets ioner, natriumioner (Na+) og hydroxidioner (OH-). Dette betyder, at næsten alle NaOH -molekyler går i stykker i ioner, i modsætning til svage baser, som kun delvist adskiller sig.
* Høj hydroxidionkoncentration: Den komplette dissociation af NaOH fører til en høj koncentration af hydroxidioner (OH-) i opløsning. Disse hydroxidioner er ansvarlige for de grundlæggende egenskaber ved opløsningen, såsom dens evne til at acceptere protoner (H+) og øge pH.
* Høj ligevægtskonstant (KB): Ligevægtskonstanten til dissociation af NaOH i vand er ekstremt stor. Dette indikerer, at reaktionen favoriserer dannelsen af ioner, hvilket yderligere understøtter ideen om fuldstændig dissociation.
I modsætning til svage baser, som kun delvist dissocierede, stærke baser som NaOH dissocierer fuldstændigt, hvilket resulterer i en signifikant højere koncentration af hydroxidioner og en stærkere grundlæggende effekt.
Sidste artikelHvad er et element, der ikke danner forbindelse?
Næste artikelHvorfor fremstiller klor en ionisk forbindelse med brom?
 Varme artikler
Varme artikler
-
 En ny løsning til spildevandsrensningKredit:Pixabay/CC0 Public Domain Syntetiske farvestoffer bruges på tværs af en lang række industrier og udgør en alvorlig bekymring, når det kommer til vandforurening. Disse farvestoffer er ikke ku
En ny løsning til spildevandsrensningKredit:Pixabay/CC0 Public Domain Syntetiske farvestoffer bruges på tværs af en lang række industrier og udgør en alvorlig bekymring, når det kommer til vandforurening. Disse farvestoffer er ikke ku -
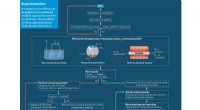 Forskere giver vejledning om nitrogenaktivering ved reduktion og oxidationEn generel protokol for N2-reduktion og oxidationseksperimenter. Kredit:ZHANG Xilun Kvælstof er afgørende for alle former for liv. Den formidable styrke af N≡N triple binding gør N 2 fiksering i
Forskere giver vejledning om nitrogenaktivering ved reduktion og oxidationEn generel protokol for N2-reduktion og oxidationseksperimenter. Kredit:ZHANG Xilun Kvælstof er afgørende for alle former for liv. Den formidable styrke af N≡N triple binding gør N 2 fiksering i -
 Papirbaseret teknologi fremmer tidligere opdagelse af kræftWenji Dong. Kredit:WSU Forskere fra Washington State University har udviklet en teknologi, der er mere end 30 gange mere følsom end nuværende laboratoriebaserede tests til at finde biomarkører for
Papirbaseret teknologi fremmer tidligere opdagelse af kræftWenji Dong. Kredit:WSU Forskere fra Washington State University har udviklet en teknologi, der er mere end 30 gange mere følsom end nuværende laboratoriebaserede tests til at finde biomarkører for -
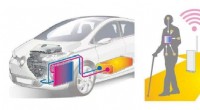 Skønhed i ufuldkommenhed:Hvordan krystaldefekter kan hjælpe med at omdanne spildvarme til elektric…Eksempler på anvendelser af elproduktion ved hjælp af termoelektrisk konvertering. Det involverer konvertering af udstødningsvarme fra bilmotorer til elektricitet til genbrug, eller bruge forskellen i
Skønhed i ufuldkommenhed:Hvordan krystaldefekter kan hjælpe med at omdanne spildvarme til elektric…Eksempler på anvendelser af elproduktion ved hjælp af termoelektrisk konvertering. Det involverer konvertering af udstødningsvarme fra bilmotorer til elektricitet til genbrug, eller bruge forskellen i
- Tidlige amerikanske astronauter stod over for usikkerhed, fare og død
- Hvilken af følgende er et eksempel på bifangst?
- Hvad er naturligt udvælgelse Hvordan driver det evolution?
- Hvad bruger forskere til at repræsentere ting, de ikke direkte kan studere?
- En ny undersøgelse viser, at vineksperter er forskellige fra geografisk område
- Hvor kan vi finde geotermisk?


