Hvad dannes kobber II -klorid og aluminium, når de kombineres?
Her er den afbalancerede kemiske ligning:
3Cucl₂ + 2Al → 2Alcl₃ + 3Cu
Forklaring:
* Aluminium er mere reaktiv end kobber, hvilket betyder, at det kan fortrænge kobber fra dets sammensætning.
* Aluminiumatomerne mister elektroner og bliver al³⁺ -ioner, mens kobberioner (Cu²⁺) får elektroner og bliver kobberatomer.
* Reaktionen er eksoterm, hvilket betyder, at den frigiver varme.
Observationer:
* Du vil observere et rødbrunt fast stof (kobber), der dannes på overfladen af aluminiumet.
* Opløsningen ville blive farveløs, hvis kobber (II) -chloridet oprindeligt blev opløst i vand.
Bemærk: Denne reaktion bruges ofte i demonstrationer som et visuelt eksempel på enkeltfortrængningsreaktioner.
 Varme artikler
Varme artikler
-
 Nye katalysatorer til bedre brændselscellerProfessor Sangaraju Shanmugam (tv) og ph.d. Student Arumugam Sivanantham (højre). Kredit:Daegu Gyeongbuk Institute of Science and Technology (DGIST) Forskere ved Daegu Gyeongbuk Institute of Scien
Nye katalysatorer til bedre brændselscellerProfessor Sangaraju Shanmugam (tv) og ph.d. Student Arumugam Sivanantham (højre). Kredit:Daegu Gyeongbuk Institute of Science and Technology (DGIST) Forskere ved Daegu Gyeongbuk Institute of Scien -
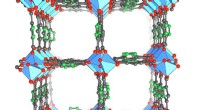 I ørkenforsøg, næste generations vandopsamler leverer frisk vand fra luftenKrystalstrukturen af de nyeste, aluminiumsbaseret metal-organisk ramme, MOF-303, som fanger dobbelt så meget vand som den tidligere MOF, der blev brugt i vandhøsteren. Kredit:Yaghi lab, UC Berkeley
I ørkenforsøg, næste generations vandopsamler leverer frisk vand fra luftenKrystalstrukturen af de nyeste, aluminiumsbaseret metal-organisk ramme, MOF-303, som fanger dobbelt så meget vand som den tidligere MOF, der blev brugt i vandhøsteren. Kredit:Yaghi lab, UC Berkeley -
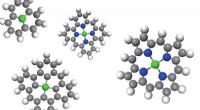 Simpel ligning styrer skabelsen af ren-energi katalysatorerTilpasset fra figur i Nature Catalysis / Springer Nature. Kredit:University of Nebraska-Lincoln Nye retningslinjer fastsat af Nebraska og kinesiske forskere kunne styre designet af billigere, mere
Simpel ligning styrer skabelsen af ren-energi katalysatorerTilpasset fra figur i Nature Catalysis / Springer Nature. Kredit:University of Nebraska-Lincoln Nye retningslinjer fastsat af Nebraska og kinesiske forskere kunne styre designet af billigere, mere -
 En intelligent, formformende, selvhelbredende materiale til integreret kunstig muskel og nervevævForskere udvikler et formformende materiale med en hidtil uset multifunktionalitet til blød robotik og bærbar elektronik. Kredit:Soft Machines Lab, Carnegie Mellon University Fremskridt inden for
En intelligent, formformende, selvhelbredende materiale til integreret kunstig muskel og nervevævForskere udvikler et formformende materiale med en hidtil uset multifunktionalitet til blød robotik og bærbar elektronik. Kredit:Soft Machines Lab, Carnegie Mellon University Fremskridt inden for
- Forskere opdager, hvordan influenzavirus kaprer menneskelige celler
- For nanomedicin, cellekøn betyder noget
- Hvorfor er Brom Polar?
- Hurtig, let, og meget følsom arsendetektion med guldnanopartikler
- Grafisk australsk video af japansk hvalfangst frigivet
- Hvad er acceleration på 8 kg masse, hvis to kræfter F1 og F2 fungerer objektet, hvor det er lig me…


