Hvorfor kaliumpermanganat er misfarvet i nærvær af 1-butanol 2-butanol, men syrer langsomt med 2-methyl-2-propanol, selvom alle tre alkoholer har samme molekylære formel?
Nøglen:Oxidation og struktur
* kmno4 som oxidisator: Kaliumpermanganat er et kraftfuldt oxidationsmiddel. Den accepterer let elektroner, hvilket får andre molekyler til at miste elektroner (blive oxideret).
* Alkoholer og oxidation: Alkoholer kan oxideres afhængigt af typen af alkohol og forholdene. Primære alkoholer kan oxideres til aldehyder og derefter til carboxylsyrer, mens sekundære alkoholer kan oxideres til ketoner. Tertiære alkoholer er generelt resistente over for oxidation.
Lad os nedbryde hver alkohol:
* 1-butanol (primær alkohol): KMNO4 oxideres hurtigt 1-butanol, hvilket fører til en farveændring fra den lilla af KmnO4 til den brune MnO2 (mangandioxid). Reaktionen fortsætter hurtigt, da den primære alkohol let danner et aldehyd.
* 2-butanol (sekundær alkohol): KMNO4 oxideres også 2-butanol, hvilket fører til en lignende farveændring. Imidlertid er reaktionen typisk langsommere end med 1-butanol. Dette skyldes, at sekundære alkoholer oxideres til ketoner, og reaktionsmekanismen er lidt mere kompleks.
* 2-methyl-2-propanol (tertiær alkohol): Denne alkohol er resistent over for oxidation af KMNO4 under normale forhold. Det tertiære carbonatom er bundet til tre andre carbonatomer, hvilket gør det vanskeligt at fjerne et hydrogenatom og danne en carbocation (et nødvendigt mellemprodukt til oxidation). Mens der kan forekomme en vis langsom forsuring på grund af tilstedeværelsen af spor af urenheder eller andre faktorer, finder den primære reaktion af oxidation ikke sted.
Kortfattet
Forskellen i reaktivitet med KMNO4 stammer fra de forskellige strukturer af disse isomere alkoholer og deres modtagelighed for oxidation. Primære alkoholer oxideres let, sekundære alkoholer oxideres i en langsommere hastighed, og tertiære alkoholer er i det væsentlige inerte for oxidation af KMNO4 under normale forhold.
Sidste artikelHvad er oxidationsantal Bro3?
Næste artikelHvorfor acetoacetic ester giver ferrisk chlorid -test?
 Varme artikler
Varme artikler
-
 Forsvindende handling:Enheden forsvinder på kommando efter militære missionerEn polymer (venstre) depolymeriserer og forsvinder efter at have været udsat for sollys i 10 minutter (højre). Kredit:Paul Kohl En polymer, der selvdestruerer? Mens engang en fiktiv idé, Der finde
Forsvindende handling:Enheden forsvinder på kommando efter militære missionerEn polymer (venstre) depolymeriserer og forsvinder efter at have været udsat for sollys i 10 minutter (højre). Kredit:Paul Kohl En polymer, der selvdestruerer? Mens engang en fiktiv idé, Der finde -
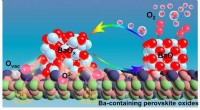 Mekanisme for oxygenaktivering på bariumholdige perovskitmaterialerOxygenaktiveringsmekanisme på Ba-holdige perovskitoxider. Kredit:Zhu Yue Et forskerhold ledet af prof. Yang Weishen og prof. Zhu Xuefeng fra Dalian Institute of Chemical Physics (DICP) fra det kine
Mekanisme for oxygenaktivering på bariumholdige perovskitmaterialerOxygenaktiveringsmekanisme på Ba-holdige perovskitoxider. Kredit:Zhu Yue Et forskerhold ledet af prof. Yang Weishen og prof. Zhu Xuefeng fra Dalian Institute of Chemical Physics (DICP) fra det kine -
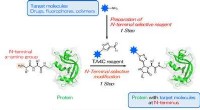 Enkel N-terminal modifikation af proteiner i et enkelt trinFig. 1. Et et-trins præparat af TA4C og en et-trins biokonjugering målrettet mod en N-terminal a-aminogruppe. Den blå stjerne repræsenterer et målmolekyle for N-terminal modifikation. Kredit:Osaka Uni
Enkel N-terminal modifikation af proteiner i et enkelt trinFig. 1. Et et-trins præparat af TA4C og en et-trins biokonjugering målrettet mod en N-terminal a-aminogruppe. Den blå stjerne repræsenterer et målmolekyle for N-terminal modifikation. Kredit:Osaka Uni -
 Teknologi afslører tidligere upåviselig proteinsignalaktivitet i diabetes, KræftKredit:Analytisk kemi, maj 2019 Proteiner er cellens arbejdsheste. Deres aktivitet styres ofte ved at tilføje eller fjerne kemikalier kaldet fosfater, som at tænde eller slukke for en elektrisk st
Teknologi afslører tidligere upåviselig proteinsignalaktivitet i diabetes, KræftKredit:Analytisk kemi, maj 2019 Proteiner er cellens arbejdsheste. Deres aktivitet styres ofte ved at tilføje eller fjerne kemikalier kaldet fosfater, som at tænde eller slukke for en elektrisk st
- Hvorfor er der græs?
- Hvor effektivt vil forskellige amerikanske skove fjerne atmosfærisk kulstof i fremtiden
- Hvad er spin på en planet eller måne, som det ses ovenfra planeter pol?
- Kamplinjer dannes forud for en truende amerikansk privatlivslovkamp
- Nyt værktøj giver forudsigelser om bølgeoversvømmelser for West Maui
- Tornado gyder østlige amerikanske storme undersøgt af GPM-satellit


