Hvad er reaktiviteten af cæsium?
* lav ioniseringsenergi: Cesium har den laveste ioniseringsenergi for alle elementer, hvilket betyder, at den let mister sin yderste elektron til at blive en positivt ladet ion (CS+). Dette gør det meget tilbøjeligt til at reagere med andre stoffer.
* stor atomradius: Cesium har en stor atomradius, hvilket betyder, at dens yderste elektron er længere væk fra kernen og holdes mindre tæt. Dette gør det lettere at fjerne elektronet og bidrage til dets høje reaktivitet.
* Elektropositivitet: Cesium er meget elektropositiv, hvilket betyder, at det har en stærk tendens til at miste elektroner og danne positive ioner.
reaktioner og egenskaber:
* reagerer med vand: Cesium reagerer eksplosivt med vand og frigiver en stor mængde varme og brintgas. Denne reaktion er endnu mere energisk end reaktionen fra andre alkalimetaller som natrium og kalium.
* reagerer med ilt: Cesium reagerer med ilt i luft til dannelse af cæsiumoxid (CS₂O) og eksploderer endda i rent ilt.
* reagerer med halogener: Cesium reagerer let med halogener (fluor, klor, brom, iod) for at danne cesiumhalogenider.
* reagerer med syrer: Cesium reagerer voldsomt med syrer og frigiver brintgas.
sikkerhed:
* Ekstrem reaktivitet: Cesium er så reaktiv, at det skal håndteres med ekstrem forsigtighed. Det opbevares normalt under inerte atmosfærer for at forhindre kontakt med luft og fugt.
* eksplosive reaktioner: Reaktionerne fra cæsium med vand, ilt og andre stoffer er meget eksoterm og kan være eksplosive.
Ansøgninger:
På trods af sin høje reaktivitet har Cesium nogle applikationer i:
* atomur: Caesium-133 bruges i atomur, som er utroligt præcise tidtagerindretninger.
* olieudforskning: Cesiumforbindelser bruges til olieudforskning til at identificere olie- og gasaflejringer.
I resuméet skyldes Cesiums høje reaktivitet dens lave ioniseringsenergi, stor atomradius og elektropositivitet. Det er det mest reaktive element på den periodiske tabel og kræver omhyggelig håndtering på grund af dets eksplosive reaktioner med forskellige stoffer.
 Varme artikler
Varme artikler
-
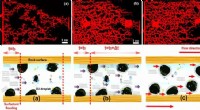 En ny klasse af forgrenede enkeltkædede overfladeaktive stoffer til forbedret olieudvinding rapport…Øverst:Forskelle i bevægelsen af olie gennem mikrokanalerne efter opløsningens oversvømmelse af (a) ren saltlage, b) rent overfladeaktivt stof og (c) overfladeaktivt middel-saltvand. Nederst:Skemati
En ny klasse af forgrenede enkeltkædede overfladeaktive stoffer til forbedret olieudvinding rapport…Øverst:Forskelle i bevægelsen af olie gennem mikrokanalerne efter opløsningens oversvømmelse af (a) ren saltlage, b) rent overfladeaktivt stof og (c) overfladeaktivt middel-saltvand. Nederst:Skemati -
 Forskere opdager superelastisk formhukommelsesmaterialeMaterialevidenskab og ingeniørprofessor Seok-Woo Lee og kolleger har opdaget superelastiske formhukommelsesegenskaber i et materiale, der kunne bruges under de hårdeste forhold, såsom det ydre rum. Kr
Forskere opdager superelastisk formhukommelsesmaterialeMaterialevidenskab og ingeniørprofessor Seok-Woo Lee og kolleger har opdaget superelastiske formhukommelsesegenskaber i et materiale, der kunne bruges under de hårdeste forhold, såsom det ydre rum. Kr -
 Den nuværende model til opbevaring af atomaffald er ufuldstændigKredit:CC0 Public Domain De materialer, USA og andre lande planlægger at bruge til at opbevare atomaffald på højt niveau, vil sandsynligvis nedbrydes hurtigere end nogen tidligere kendte på grund
Den nuværende model til opbevaring af atomaffald er ufuldstændigKredit:CC0 Public Domain De materialer, USA og andre lande planlægger at bruge til at opbevare atomaffald på højt niveau, vil sandsynligvis nedbrydes hurtigere end nogen tidligere kendte på grund -
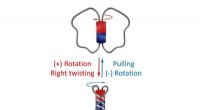 Alle afviklede:En reversibel molekylær hvirvelDenne molekylære hvirvel kan vrides reversibelt, og forskere kan måle dens kræfter. Kredit:Tilpasset fra Journal of the American Chemical Society (2022), DOI:10.1021/jacs.2c02547 I løbet af de sids
Alle afviklede:En reversibel molekylær hvirvelDenne molekylære hvirvel kan vrides reversibelt, og forskere kan måle dens kræfter. Kredit:Tilpasset fra Journal of the American Chemical Society (2022), DOI:10.1021/jacs.2c02547 I løbet af de sids
- SmartFarm-enhed høster luftfugtighed for autonom, selvbærende bylandbrug
- En ud af seks historiske ressourcer i Colorado er i en flodslette
- Forskere forestiller kvasipartikler, der kan føre til hurtigere kredsløb, højere båndbredder
- Forskere anvender eksperimentel økonomi til mexicansk vandmangel
- Historiefortælling i metaversen kan anspore miljøhandlinger
- Hvad kaldes antallet af elektroner i den ydre skal?


