Hvad er resultaterne fra AL -reaktionen med Koh?
Her er den afbalancerede kemiske ligning:
2 Al + 2 Koh + 6 H 2 O → 2 kalo 2 + 3 h 2 ↑
Forklaring:
* aluminium (AL) er et reaktivt metal.
* kaliumhydroxid (KOH) er en stærk base.
* I nærvær af vand forekommer reaktionen.
* Aluminiumet reagerer med hydroxidionerne (OH-) fra KOH til dannelse af kaliumaluminat (Kalo 2 ).
* Reaktionen frigiver også brintgas (H 2 ), hvorfor du ser bobler dannes.
Nøglepunkter:
* Denne reaktion er et eksempel på en forskydningsreaktion .
* Reaktionen er eksoterm , hvilket betyder, at det frigiver varme.
* Reaktionen bruges i den kommercielle produktion af aluminiumshydroxid (AL (OH) 3 ).
* Reaktionen bruges også i rengøring af aluminiumsoverflader Fordi det fjerner oxidlaget, der dannes på aluminium.
sikkerhed:
* Denne reaktion er meget eksoterm , så håndter det med forsigtighed.
* Bær passende sikkerhedsudstyr, inklusive handsker og øjenbeskyttelse.
* Arbejd i et godt ventileret område.
Sidste artikelHvorfor kan vand opløses så mange forbindelser?
Næste artikelHvilken type bindinger mellem svovl- og iltatomer?
 Varme artikler
Varme artikler
-
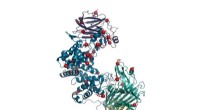 Omkonstrueret enzym kan hjælpe med at vende skader fra rygmarvsskade og slagtilfældeI denne gengivelse af enzymet chondroitinase ABC, punktmutationer repræsenteres af røde kugler. Denne re-manipulerede form af enzymet er mere stabil og mere aktiv end vildtypen og kan bruges til at hj
Omkonstrueret enzym kan hjælpe med at vende skader fra rygmarvsskade og slagtilfældeI denne gengivelse af enzymet chondroitinase ABC, punktmutationer repræsenteres af røde kugler. Denne re-manipulerede form af enzymet er mere stabil og mere aktiv end vildtypen og kan bruges til at hj -
 Et periodisk system med molekylære knuderHvilke nye knudetyper vil det være muligt at realisere i fremtiden? Dette er det udfordrende spørgsmål, som SISSA -forskere, i samarbejde med University of Padua, har tacklet ved hjælp af computersimu
Et periodisk system med molekylære knuderHvilke nye knudetyper vil det være muligt at realisere i fremtiden? Dette er det udfordrende spørgsmål, som SISSA -forskere, i samarbejde med University of Padua, har tacklet ved hjælp af computersimu -
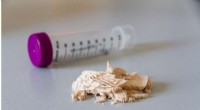 Bakterier fodret på en tilpasset diæt producerer biologisk nedbrydelige polymerer til alternativ e…Frysetørrede bakterier (Cupriavidus necator) før celleafbrydelse. Kredit:Fraunhofer-Gesellschaft Tyskland genererer omkring 38 kg plastaffald pr. indbygger hvert år. I et fælles projekt med Univer
Bakterier fodret på en tilpasset diæt producerer biologisk nedbrydelige polymerer til alternativ e…Frysetørrede bakterier (Cupriavidus necator) før celleafbrydelse. Kredit:Fraunhofer-Gesellschaft Tyskland genererer omkring 38 kg plastaffald pr. indbygger hvert år. I et fælles projekt med Univer -
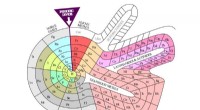 Det periodiske system er 150 - men det kunne have set meget anderledes udTheodor Benfeys spirabord (1964). Kredit:DePiep/Wikipedia Det periodiske system stirrer ned fra væggene i næsten alle kemilaboratorier. Æren for dens oprettelse går generelt til Dimitri Mendeleev,
Det periodiske system er 150 - men det kunne have set meget anderledes udTheodor Benfeys spirabord (1964). Kredit:DePiep/Wikipedia Det periodiske system stirrer ned fra væggene i næsten alle kemilaboratorier. Æren for dens oprettelse går generelt til Dimitri Mendeleev,
- Molekylære vibrationer reducerer den maksimalt opnåelige fotovoltage i organiske solceller
- Oversætte humoristisk børnedigtning? Indholdet betyder mest
- Er magnetisme en kilde til grøn energi?
- Hvilket proteinkompleks absorberer den energi, der bruges til at producere NADPH?
- Hvad er bidrag fra Hertz i elektromagnetisk?
- Hvad er også kendt af en termisk energi?


