Forskel i opløseligheden af ciprofloxacin-vand og 0,1N HCI-opløsning I-E. Jeg mener at bede om, at enten eller 0,1 N er mere opløselig?
* ciprofloxacins struktur: Ciprofloxacin er en svag base. Det har en grundlæggende amingruppe, der kan blive protoneret (få en hydrogenion, H+) i sure opløsninger.
* opløselighed og pH: Opløseligheden af svage baser er meget pH-afhængig.
* I sure opløsninger (som 0,1 N HCI) bliver amingruppen af ciprofloxacin protoneret, hvilket danner en positivt ladet art.
* Denne positivt ladede form for ciprofloxacin er mere opløselig i vand end den neutrale form.
* Vand: I rent vand er pH -værdien neutral, og kun en lille del af ciprofloxacin -molekyler vil blive protoneret. Dette begrænser dens opløselighed.
Kortfattet:
* 0,1 N HCL: Det sure miljø protonerer ciprofloxacin og øger dets opløselighed.
* Vand: Den neutrale pH resulterer i mindre protonation og lavere opløselighed.
Vigtig note: Mens ciprofloxacin er mere opløselig i sure opløsninger, afhænger den faktiske opløselighed af den specifikke koncentration af HCL -opløsningen og temperaturen.
Sidste artikelHvor mange atomer af hver type er i 4HNO3?
Næste artikelHvad er formbarheden af brint?
 Varme artikler
Varme artikler
-
 Designerbakterier producerer koralantibiotikaHornkoraller af arten Antillogorgia elisabethae producerer antibiotiske naturlige stoffer. Et forskerhold på TUM har med succes produceret et af disse stoffer i laboratoriet. Kredit:Thomas Brück/TUM
Designerbakterier producerer koralantibiotikaHornkoraller af arten Antillogorgia elisabethae producerer antibiotiske naturlige stoffer. Et forskerhold på TUM har med succes produceret et af disse stoffer i laboratoriet. Kredit:Thomas Brück/TUM -
 Titan-i-et-glas-eksperimenter antyder mineralsammensætning af Saturn-månenÆgte farvebillede af lag af dis i Titans atmosfære. Kredit:NASA Titan, Saturns største måne, er et naturligt laboratorium til at studere livets oprindelse. Ligesom Jorden, Titan har en tæt atmosfæ
Titan-i-et-glas-eksperimenter antyder mineralsammensætning af Saturn-månenÆgte farvebillede af lag af dis i Titans atmosfære. Kredit:NASA Titan, Saturns største måne, er et naturligt laboratorium til at studere livets oprindelse. Ligesom Jorden, Titan har en tæt atmosfæ -
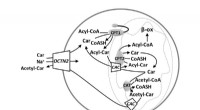 OCTN:En transportør med relevans for human patofysiologi, opdagelse og diagnostik af lægemidlerOCTN:En lille transportfamilie med stor relevans for menneskelig patofysiologi, Drug Discovery and Diagnostics Credit:Cesare Indiveri I februar 2019 -udgaven af SLAS Discovery , en gennemgang af
OCTN:En transportør med relevans for human patofysiologi, opdagelse og diagnostik af lægemidlerOCTN:En lille transportfamilie med stor relevans for menneskelig patofysiologi, Drug Discovery and Diagnostics Credit:Cesare Indiveri I februar 2019 -udgaven af SLAS Discovery , en gennemgang af -
 Kemikere udvikler kontaminantdetekteringsteknik for heparinJason Dwyer, lektor i kemi, taler med James Hagan, fra Nashua, N.H., en doktorand i Dwyers forskningsgruppe, og gymnasieelev Anna Khabaeva, fra Cranston, der er på et forskningsstipendium. Kredit:Mich
Kemikere udvikler kontaminantdetekteringsteknik for heparinJason Dwyer, lektor i kemi, taler med James Hagan, fra Nashua, N.H., en doktorand i Dwyers forskningsgruppe, og gymnasieelev Anna Khabaeva, fra Cranston, der er på et forskningsstipendium. Kredit:Mich
- Hubbles mest følsomme billeder viser fjerne galakser
- Halloween er en vigtig måde at tænke døden på
- Hvad producerer temperaturforskelle mellem ækvator og to poler?
- Hvad er den nyttige energi i en fløjte?
- Hvilken slags pc kan komme i en cabriolet eller skiferform?
- Atomfusionsprojekt står over for forsinkelser over amerikanske budgetnedskæringer:direktør


