Hvad ville være molariteten af en 5 procent NaCl -løsning?
1. Forståelse af terminologien
* 5% NaCl -løsning: Dette betyder, at der er 5 gram NaCI (natriumchlorid) i hver 100 gram opløsning.
* Molaritet: Molaritet (M) defineres som antallet af mol opløst stof pr. Liter opløsning.
2. Beregninger
* Trin 1:Konverter gram NaCl til mol.
* Molekylvægten af NaCI er ca. 58,44 g/mol.
* Mol NaCl =(5 g NaCl) / (58,44 g / mol) =0,0855 mol NaCl
* Trin 2:Beregn volumenet af opløsningen i liter.
* Hvis man antager en densitet på 1 g/ml for opløsningen (som er tæt på fortyndede opløsninger), svarer 100 gram opløsning til 100 ml.
* Konverter ml til liter:100 ml =0,1 l
* Trin 3:Beregn molariteten.
* Molaritet (M) =(mol NaCl) / ((lydstyrke af liter)
* M =(0,0855 mol) / (0,1 l) =0,855 m
Derfor har en 5% NaCl -løsning en molaritet på ca. 0,855 m.
Vigtige noter:
* Løsningen af opløsningen kan variere lidt afhængigt af temperaturen. For mere præcise beregninger skal du kende den specifikke densitet af din 5% NaCl -løsning.
* Denne beregning antager, at 5% -koncentrationen er vægt/vægt (w/w). Hvis det er vægt/volumen (w/v), ville beregningen være lidt anderledes.
Sidste artikelFind antallet af mol i 564 gram kobber?
Næste artikelHvordan vil du adskille en blanding af brint og klor?
 Varme artikler
Varme artikler
-
 Video:Hvordan bly (måske) forårsagede det gamle Roms undergangKredit:The American Chemical Society Det antikke Roms kejsere lavede nogle ret bizarre ting - brast ud i ukontrollable latteranfald, udnævne en hest til præst, klæder sig i dyreskind og angriber m
Video:Hvordan bly (måske) forårsagede det gamle Roms undergangKredit:The American Chemical Society Det antikke Roms kejsere lavede nogle ret bizarre ting - brast ud i ukontrollable latteranfald, udnævne en hest til præst, klæder sig i dyreskind og angriber m -
 Ramme til at spore individuelle kulstofatomers vejKredit:CC0 Public Domain Som vandmolekyler i en flod, jordens kulstofatomer er altid i bevægelse. For bedre at forstå denne handling, Lawrence Livermore National Laboratory (LLNL) forskere og sam
Ramme til at spore individuelle kulstofatomers vejKredit:CC0 Public Domain Som vandmolekyler i en flod, jordens kulstofatomer er altid i bevægelse. For bedre at forstå denne handling, Lawrence Livermore National Laboratory (LLNL) forskere og sam -
 Videnskab ved grænsefladen:Bioinspirerede materialer afslører nyttige egenskaberNy forskning af Brian Wadsworth, Gary Moore og deres kolleger pryder forsiden af tidsskriftet ACS Materials &Interfaces. Inspireret af naturen, hvor aminosyrerester og bløde materialers koordination
Videnskab ved grænsefladen:Bioinspirerede materialer afslører nyttige egenskaberNy forskning af Brian Wadsworth, Gary Moore og deres kolleger pryder forsiden af tidsskriftet ACS Materials &Interfaces. Inspireret af naturen, hvor aminosyrerester og bløde materialers koordination -
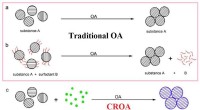 Nyt stof kan dannes i den orienterede vedhæftningsproces med krystalvækst, undersøgelse afslører1a, Traditionel orienteret fastgørelse (OA) af nanopartikler for at danne en enkelt krystal. Fig. 1b, Ved hjælp af overfladeaktive stoffer (røde bølgede linjer) kan der også dannes en enkelt krystal v
Nyt stof kan dannes i den orienterede vedhæftningsproces med krystalvækst, undersøgelse afslører1a, Traditionel orienteret fastgørelse (OA) af nanopartikler for at danne en enkelt krystal. Fig. 1b, Ved hjælp af overfladeaktive stoffer (røde bølgede linjer) kan der også dannes en enkelt krystal v
- Kamp opad:Spaniens vinproducenter tilpasser sig klimaændringerne
- Uberørte antarktiske fjorde indeholder tilsvarende niveauer af mikroplast som åbne oceaner nær st…
- Hvordan ændrer tiden for planeten til kredsløb solen med sin afstand fra solen?
- Hvorfor er vind en god energikilde?
- Første videnskab med ALMAs højeste frekvensegenskaber
- Hvem opdagede Jupiter først?


