Hvordan kombinerer du kulstof og klor?
Hvorfor direkte kombination er vanskelig:
* Carbon's stabilitet: Carbon er et meget stabilt element. Det danner stærke kovalente bindinger med sig selv (som i diamant eller grafit) og med andre elementer som brint (som i kulbrinter).
* klorens reaktivitet: Chlor er en meget reaktiv ikke -metal. Det reagerer let med metaller for at danne salte, men danner ikke let stabile bindinger med kulstof.
Metoder til kombination af kulstof og klor:
1. Substitutionsreaktioner:
* Du kan introducere kloratomer til organiske forbindelser (forbindelser, der indeholder kulstof og brint) ved hjælp af substitutionsreaktioner .
* Et almindeligt eksempel er klorering af metan (CH4):
`` `
CH4 + CL2 → CH3CL + HCL
`` `
* Denne reaktion initieres ofte af UV -lys eller varme, og den involverer udskiftning af et hydrogenatom i methan med et kloratom.
2. Tilføjelsesreaktioner:
* Nogle umættede kulbrinter (indeholdende dobbelt- eller tredobbeltbindinger) kan gennemgå Tilføjningsreaktioner med klor.
* For eksempel reagerer ethen (C2H4) med klor til dannelse af 1,2-dichlorethan:
`` `
C2H4 + CL2 → CH2CLCH2CL
`` `
3. frie radikale reaktioner:
* Frie radikale reaktioner kan bruges til at introducere klor i kulstofkæder. Dette involverer ofte anvendelse af frie radikale initiativtagere (som peroxider) og specifikke reaktionsbetingelser.
4. organometalliske forbindelser:
* Organometalliske forbindelser, såsom Grignard-reagenser (R-MGX, hvor R er en organisk gruppe, og X er et halogen), kan bruges til at reagere med chlorholdige molekyler til at introducere chloratomer i organiske molekyler.
Vigtige overvejelser:
* reaktionsbetingelser: De specifikke reaktionsbetingelser (temperatur, lys, katalysatorer) er afgørende for at opnå den ønskede reaktion og produkt.
* sikkerhed: Klor er en giftig gas, så disse reaktioner bør udføres med passende sikkerhedsforholdsregler.
Fortæl mig, hvis du har andre spørgsmål!
 Varme artikler
Varme artikler
-
 Kunstig fotosyntese kan omdanne ubrugelig kuldioxid til myresyre, der bruges i industrienNaturlig fotosyntese er ikke altid særlig effektiv. Når videnskabsmænd efterligner det, de forsøger at gøre processerne meget mere effektive. Kredit:Colourbox Med energi fra solen, et særligt enzy
Kunstig fotosyntese kan omdanne ubrugelig kuldioxid til myresyre, der bruges i industrienNaturlig fotosyntese er ikke altid særlig effektiv. Når videnskabsmænd efterligner det, de forsøger at gøre processerne meget mere effektive. Kredit:Colourbox Med energi fra solen, et særligt enzy -
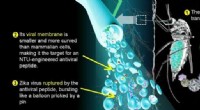 Peptid udnytter akilleshælen fra Zika-virusIllustration af forskningsresultatet. Kredit:NTU Singapore Forskere ved Nanyang Technological University, Singapore (NTU Singapore) har udviklet et antiviralt peptid, der udnytter Zika-virussen ve
Peptid udnytter akilleshælen fra Zika-virusIllustration af forskningsresultatet. Kredit:NTU Singapore Forskere ved Nanyang Technological University, Singapore (NTU Singapore) har udviklet et antiviralt peptid, der udnytter Zika-virussen ve -
 Forsker arbejder på at forstå, hvordan gonoré udvikler resistens over for antibiotikaDette billede genereret ved røntgenkrystallografi viser et cephalosporin-antibiotikum, i pink, binding til et protein fra bakterien, der forårsager gonoré. Kuglerne repræsenterer vandmolekyler. Kredit
Forsker arbejder på at forstå, hvordan gonoré udvikler resistens over for antibiotikaDette billede genereret ved røntgenkrystallografi viser et cephalosporin-antibiotikum, i pink, binding til et protein fra bakterien, der forårsager gonoré. Kuglerne repræsenterer vandmolekyler. Kredit -
 Den schweiziske hærkniv af røgskærmeEn ny type røggranat, der kan skjule sensorer i det synlige og infrarøde område, brænder under en test. Kredit:US Army At udløse røgbomber er mere end god fornøjelse den fjerde juli. Militæret bru
Den schweiziske hærkniv af røgskærmeEn ny type røggranat, der kan skjule sensorer i det synlige og infrarøde område, brænder under en test. Kredit:US Army At udløse røgbomber er mere end god fornøjelse den fjerde juli. Militæret bru
- Ny forståelse af kenyanske palæmiljøer åbner vindue om menneskelig udvikling i området
- Hvad er krukkenes slette?
- Overførsel af en dominoreaktion ved hjælp af redoxkemi opnået for første gang
- UK rumskrot-projekt fremhæver trussel mod missioner
- Hvorfor kunne et dysfunktionelt gen påvirke en type celle i kroppen, men ikke andre typer?
- Ny type supercomputer kunne være baseret på en magisk støvkombination af lys og stof


