Hvad sker der, når saltsyre reagerer med ammoniumhydroxid Er dette en exothetermisk eller endotermisk?
Reaktionen er eksoterm.
Her er hvorfor:
* neutraliseringsreaktioner: Neutraliseringsreaktioner involverer reaktionen af en syre og en base, der frigiver varme. Dette skyldes, at dannelsen af salt (ammoniumchlorid i dette tilfælde) og vand er en mere stabil tilstand end den separate syre og base.
* varmefrigivelse: Den varme, der frigives under reaktionen, er drivkraften bag processen. Du vil sandsynligvis observere en stigning i temperaturen, hvis du skulle blande disse løsninger.
Kemisk ligning:
HCL (aq) + nh₄OH (aq) → NH₄CL (aq) + h₂o (l) + varme
Vigtig note: Mens ammoniumhydroxid ofte bruges som et udtryk, er det vigtigt at forstå, at det ikke findes som en tydelig forbindelse i opløsningen. Ammoniumhydroxid er faktisk ammoniak (NH₃) opløst i vand.
 Varme artikler
Varme artikler
-
 Ny proces genbruger mere effektivt overskydende kuldioxid til brændstof, undersøgelse finderKredit:CC0 Public Domain Årevis, forskere har arbejdet på at genbruge overskydende atmosfærisk kuldioxid til nye kemikalier, brændstoffer og andre produkter, der traditionelt er fremstillet af kul
Ny proces genbruger mere effektivt overskydende kuldioxid til brændstof, undersøgelse finderKredit:CC0 Public Domain Årevis, forskere har arbejdet på at genbruge overskydende atmosfærisk kuldioxid til nye kemikalier, brændstoffer og andre produkter, der traditionelt er fremstillet af kul -
 Udskiftning af funktionelle grupper med en guldelektrode for at kontrollere et molekyles reaktivitetIBS- og KAIST-forskere brugte guldelektroden og fastgjorde målmolekylerne på elektroden. Ligesom funktionelle grupper genererer forskellige elektroniske effekter, en elektrode passer til alle reaktion
Udskiftning af funktionelle grupper med en guldelektrode for at kontrollere et molekyles reaktivitetIBS- og KAIST-forskere brugte guldelektroden og fastgjorde målmolekylerne på elektroden. Ligesom funktionelle grupper genererer forskellige elektroniske effekter, en elektrode passer til alle reaktion -
 Undersøgelse afslører ny indsigt i, hvordan hybride perovskit-solceller fungererDenne illustration viser, hvad der sker inde i et hybridt perovskitmateriale i de første par billiontedele af et sekund, efter at det er ramt af simuleret sollys (øverst til venstre). De blå og grønne
Undersøgelse afslører ny indsigt i, hvordan hybride perovskit-solceller fungererDenne illustration viser, hvad der sker inde i et hybridt perovskitmateriale i de første par billiontedele af et sekund, efter at det er ramt af simuleret sollys (øverst til venstre). De blå og grønne -
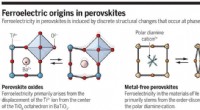 En måde at lave renere metalfrie perovskitter til en lav prisFerroelektricitet i perovskitter induceres af diskrete strukturelle ændringer, der sker ved faseovergange. Kredit:(c) C. Bickel/ Videnskab (2018). DOI:10.1126/science.aas9330 Et team af forskere
En måde at lave renere metalfrie perovskitter til en lav prisFerroelektricitet i perovskitter induceres af diskrete strukturelle ændringer, der sker ved faseovergange. Kredit:(c) C. Bickel/ Videnskab (2018). DOI:10.1126/science.aas9330 Et team af forskere
- Forskere udvikler irreversibel inhibitor til at adressere proteiner, der har erhvervet lægemiddelre…
- En Indien-Pakistan atomkrig kan dræbe millioner, true global sult
- Sort hul kollisioner kan hjælpe os med at måle, hvor hurtigt universet udvider sig
- Når man ser et objekt gennem højeffektmålet for et mikroskop, kan ikke alle objeect være i fokus…
- Hvilke partikler bidrager til ladningen af et atom?
- At adressere magtforskelle kan anspore fordelagtige racegrupper til at handle for racelighed


