Hvilket har den højere begrænsende molære ledningsevne-NaCl eller KCL, og hvad er grund?
Årsag:
Begrænsning af molær ledningsevne (λ °) er et mål for ledningsevnen af en elektrolytopløsning ved uendelig fortynding. Det repræsenterer den maksimale ledningsevne, der kan opnås ved elektrolytten, når koncentrationen nærmer sig nul.
Den begrænsende molære ledningsevne påvirkes af flere faktorer, herunder:
* ionisk mobilitet: Ioner med højere mobilitet bidrager mere til konduktiviteten.
* ionisk størrelse: Mindre ioner har en tendens til at have højere mobilitet på grund af mindre modstand mod bevægelse i opløsningen.
* Hydrering: Ioner, der er stærkere hydreret, har lavere mobilitet, fordi de er omgivet af en større skaldyrmolekyler.
I tilfælde af NaCl og KCL:
* ionisk størrelse: K⁺ioner er større end Na⁺ -ioner.
* Hydrering: K⁺ioner er mindre stærkt hydreret end Na⁺ -ioner.
Derfor:
* K⁺ioner har højere mobilitet end Na⁺ -ioner på grund af deres større størrelse og svagere hydrering.
* Cl⁻ioner har samme størrelse og hydrering i både NaCl og KCl.
Som et resultat har KCL en højere begrænsende molær ledningsevne end NaCI, fordi den højere mobilitet af K⁺ioner opvejer den lidt lavere mobilitet af Cl⁻ioner.
Eksperimentelle værdier:
* Λ ° (NaCl) =126,5 s cm² mol⁻¹
* Λ ° (KCL) =149,8 s cm² mol⁻¹
Disse eksperimentelle data bekræfter, at KCL har en højere begrænsende molær ledningsevne end NaCI.
Sidste artikelHvad reagerer med molekyler i lavere atmosfære for at producere giftstoffer?
Næste artikelHvad er farverne på blysalte?
 Varme artikler
Varme artikler
-
 ABS af molekylære motorerHarald Platta, Rebecca Brinkmeier og Thomas Mastalski (fra venstre) i laboratoriet på Ruhr-Universität Bochum. Kredit:RUB, Kramer Peroxisomer er celleorganeller, der udfører en række funktioner, h
ABS af molekylære motorerHarald Platta, Rebecca Brinkmeier og Thomas Mastalski (fra venstre) i laboratoriet på Ruhr-Universität Bochum. Kredit:RUB, Kramer Peroxisomer er celleorganeller, der udfører en række funktioner, h -
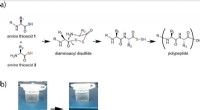 Dannelse af kunstig peptidbinding giver spor til skabelse af liv på JordenPolypeptiddannelse ved den oxidative reaktion af aminosyrer. (a) Amino thioacids 1 og 2 kobles via et diaminoacyldisulfid-mellemprodukt, og efterfølgende intramolekylær amiddannelse genererer en alfa-
Dannelse af kunstig peptidbinding giver spor til skabelse af liv på JordenPolypeptiddannelse ved den oxidative reaktion af aminosyrer. (a) Amino thioacids 1 og 2 kobles via et diaminoacyldisulfid-mellemprodukt, og efterfølgende intramolekylær amiddannelse genererer en alfa- -
 Hvordan robotmatematik og smartphones førte forskere til et gennembrud for stofopdagelseAt flytte en robot er som at manipulere et molekyle. Kredit:Willyam Bradberry/Shutterstock.com For os mennesker, en sund hjerne håndterer alle de små detaljer om kropslig bevægelse uden at kræve b
Hvordan robotmatematik og smartphones førte forskere til et gennembrud for stofopdagelseAt flytte en robot er som at manipulere et molekyle. Kredit:Willyam Bradberry/Shutterstock.com For os mennesker, en sund hjerne håndterer alle de små detaljer om kropslig bevægelse uden at kræve b -
 Forskere opdager en ny gavnlig funktion af et gammelt proteinKredit:CC0 Public Domain Cellegrænser er lavet af lipider. Når celler er alvorligt beskadiget, disse lipider skal fjernes hurtigt for at undgå toksicitet og lette heling af væv. Forskere har opdag
Forskere opdager en ny gavnlig funktion af et gammelt proteinKredit:CC0 Public Domain Cellegrænser er lavet af lipider. Når celler er alvorligt beskadiget, disse lipider skal fjernes hurtigt for at undgå toksicitet og lette heling af væv. Forskere har opdag
- Er syrer fra planter rødder, der bryder klipper en mekanisk reaktion?
- Naturlig vegetation i den ækvatoriale region?
- USA slutter sig til klimaforhandlinger trods Paris -aftalen forlader
- Klimajournalistik er stærk i hårdt ramte lande
- Hvilke 2 måder, hvorpå elektrisk ladning kan produceres?
- Sådan udvindes olie fra Flowers


