Hvad er det samlede antal valenselektroner i et fluoratom Du n jordtilstand?
Her er hvorfor:
* Elektronkonfiguration: Fluorens elektronkonfiguration er 1S² 2s² 2p⁵.
* Valence Shell: Den yderste skal (i dette tilfælde den anden skal) betragtes som valensskallen.
* Valenselektroner: Elektronerne i valensskallen er valenselektronerne, der er involveret i kemisk binding. I fluor er der 2 elektroner i 2S -underskalet og 5 elektroner i 2P -underskalet, i alt 7 valenselektroner.
 Varme artikler
Varme artikler
-
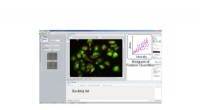 Forskere udvikler cellesugende teknologiPrikker i Histogram Feature Quantities svarer til hver celle. Vælg og klik på prikkerne på histogrammet for at bestemme, hvilke celler der skal suges. T baseret på de forudindstillede funktionsmængder
Forskere udvikler cellesugende teknologiPrikker i Histogram Feature Quantities svarer til hver celle. Vælg og klik på prikkerne på histogrammet for at bestemme, hvilke celler der skal suges. T baseret på de forudindstillede funktionsmængder -
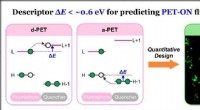 Generel beskrivelse sætter gang i fremskridt inden for farvestofkemiForskere fra SUTD, DICP, og POSTECH udviklede en teoretisk deskriptor ΔE til at forudsige PET-baserede fluorescensprober; ved at bruge denne deskriptor, de designede kvantitativt fluorescerende plette
Generel beskrivelse sætter gang i fremskridt inden for farvestofkemiForskere fra SUTD, DICP, og POSTECH udviklede en teoretisk deskriptor ΔE til at forudsige PET-baserede fluorescensprober; ved at bruge denne deskriptor, de designede kvantitativt fluorescerende plette -
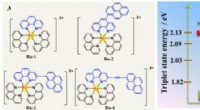 Finjustering af den exciterede tilstand af Ru(II)-fotosensibilisatorer til at øge kuldioxidomdannel…(Venstre) Molekylær struktur af Ru-1-Ru-4. (Højre) Energidiagram over triplettilstande af Ru-1, og L-2-L-4. Kredit:©Science China Press Soldrevet reduktion af CO 2 til energirige brændstoffer, s
Finjustering af den exciterede tilstand af Ru(II)-fotosensibilisatorer til at øge kuldioxidomdannel…(Venstre) Molekylær struktur af Ru-1-Ru-4. (Højre) Energidiagram over triplettilstande af Ru-1, og L-2-L-4. Kredit:©Science China Press Soldrevet reduktion af CO 2 til energirige brændstoffer, s -
 Nye molekyler for at reducere omkostningerne, miljøpåvirkning af minedrift af ædelmetallerKredit:University of Notre Dame Forskere ved University of Notre Dame har opfundet en ny klasse af molekyler, der kan bruges til at forenkle processen, der bruges til at fange ædelmetaller, herund
Nye molekyler for at reducere omkostningerne, miljøpåvirkning af minedrift af ædelmetallerKredit:University of Notre Dame Forskere ved University of Notre Dame har opfundet en ny klasse af molekyler, der kan bruges til at forenkle processen, der bruges til at fange ædelmetaller, herund
- Har fosfolipidmolekylet to dele polær ende og bipolær ende?
- Midt i Saltonhavets ødemark, en mirakuløs, men udfordrende oase er født
- Hvad er sammensætningen af uorganiske forbindelser?
- Mine efter guld med en computer
- Kode i kinesisk overvågningsapp analyseret
- Hvad kaldes en virus, der formerer sig i en bakterie?


