Hvorfor blev hydrogenperoxid ikke opvarmet før titreret med kaliumpermanganat?
* Nedbrydning: Opvarmning af brintperoxid fremskynder sin nedbrydning til vand og ilt:
2 H₂O₂ → 2 H₂O + O₂
Denne nedbrydning ville reducere koncentrationen af H₂O₂ i opløsningen, hvilket fører til unøjagtige titreringsresultater.
* reaktivitet: Mens hydrogenperoxid er et stærkt oxidationsmiddel, kan det reagere med andre stoffer, der er til stede i opløsningen, når de opvarmes, hvilket yderligere komplicerer reaktionen og gør titrering mindre pålidelig.
* sikkerhed: Opvarmning af brintperoxid kan være farligt, især i koncentrerede opløsninger. Det kan frigive brandfarlig iltgas og potentielt forårsage eksplosioner.
Hvorfor titrering udføres:
Titrering af hydrogenperoxid med kaliumpermanganat anvendes til at bestemme koncentrationen af hydrogenperoxid i en opløsning. Reaktionen er:
2 kmno₄ + 5 H₂O₂ + 3 H₂SO₄ → K₂so₄ + 2 Mnso₄ + 8 H₂O + 5 O₂
I denne reaktion reduceres permanganationen (MNO₄⁻) til Mn²⁺, mens hydrogenperoxid oxideres til ilt. Slutpunktet for titreringen nås, når opløsningen bliver permanent lyserød på grund af overskuddet af permanganationer.
Konklusion: Opvarmning af hydrogenperoxid før titrering med kaliumpermanganat er ikke anbefalet På grund af risikoen for nedbrydning, potentiel reaktivitet og sikkerhedsmæssige bekymringer. Titrering udføres typisk ved stuetemperatur for at sikre nøjagtige og sikre resultater.
Sidste artikelHvad er molariteten af opløsning, der indeholder 5,0 mol KCL i 2,0 L opløsning?
Næste artikelHvad reagerer med fosfat?
 Varme artikler
Varme artikler
-
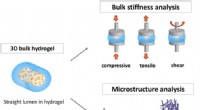 Semi-fleksibel modelbaseret analyse af celleadhæsion til hydrogelerSkematisk repræsentation af metoder til karakterisering af hydrogels fysiske egenskaber:hydrogels bulkstivhed og kædefleksibilitet i viskoelastiske netværk gennem den semi-fleksible model. Kredit: Vid
Semi-fleksibel modelbaseret analyse af celleadhæsion til hydrogelerSkematisk repræsentation af metoder til karakterisering af hydrogels fysiske egenskaber:hydrogels bulkstivhed og kædefleksibilitet i viskoelastiske netværk gennem den semi-fleksible model. Kredit: Vid -
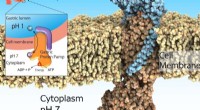 Forskere etablerer krystalstruktur af gastrisk protonpumpeDen gastriske protonpumpe, også kendt som H+, K+-ATPase, udtrykkes på overfladen af maven for at udskille mavesyren, der er uundværlig for fordøjelsen af proteiner i maden. Imidlertid, for meget s
Forskere etablerer krystalstruktur af gastrisk protonpumpeDen gastriske protonpumpe, også kendt som H+, K+-ATPase, udtrykkes på overfladen af maven for at udskille mavesyren, der er uundværlig for fordøjelsen af proteiner i maden. Imidlertid, for meget s -
 Ladningsoverførsel inden for overgangsmetalfarvestoffer analyseretEn røntgenimpuls sonderer delokaliseringen af jern-3d-elektroner på tilstødende ligander. Kredit:M. Künsting/HZB Overgangsmetalkomplekser i farvestofbaserede solceller er ansvarlige for at omdan
Ladningsoverførsel inden for overgangsmetalfarvestoffer analyseretEn røntgenimpuls sonderer delokaliseringen af jern-3d-elektroner på tilstødende ligander. Kredit:M. Künsting/HZB Overgangsmetalkomplekser i farvestofbaserede solceller er ansvarlige for at omdan -
 Forskere opdager stabilitet i hybride fotoelektriske nanomaterialerFig. 1. En computermodel af kulstofnanorør dækket af phthalocyaniner. Kredit:Pavel Krasnov Et hold af sibiriske forskere og udenlandske kolleger beregnede de parametre, der påvirker intensiteten a
Forskere opdager stabilitet i hybride fotoelektriske nanomaterialerFig. 1. En computermodel af kulstofnanorør dækket af phthalocyaniner. Kredit:Pavel Krasnov Et hold af sibiriske forskere og udenlandske kolleger beregnede de parametre, der påvirker intensiteten a
- Saturns måne Titan har jordlignende funktioner
- Hvordan opvarmer en radiator huset?
- Hvad er breddegrad og længdegrad i Baikal -søen?
- Kan din etnicitet påvirke vejrtolerancen?
- Vildmarken i en Lake Ontario-bugt afslører, hvordan kysthabitater lider under skiftende klima, menn…
- Hvad er den ædle gasnotation af Rubidium?


