Hvor mange hydrogenbindinger kan ammoniakmolekyleformer?
Her er hvorfor:
* Hydrogenbinding: Hydrogenbindinger er en type intermolekylær kraft, der forekommer mellem et hydrogenatom kovalent knyttet til et stærkt elektronegativt atom (som nitrogen, ilt eller fluor) og et ensomt par elektroner på et andet elektronegativt atom.
* ammoniakstruktur: Ammoniak har et centralt nitrogenatom med tre hydrogenatomer bundet til det. Nitrogenatomet har også et ensomt par elektroner.
* Hydrogenbindingsdannelse: Det ensomme par på nitrogenet kan danne en brintbinding med et hydrogenatom af et andet ammoniakmolekyle. Derudover kan hvert af de tre hydrogenatomer på ammoniak danne en brintbinding med det ensomme par på nitrogenet i et andet ammoniakmolekyle.
Derfor kan et ammoniakmolekyle danne et Hydrogenbinding med dets ensomme par og tre Hydrogenbindinger med sine tre hydrogenatomer, hvilket gør i alt fire Hydrogenbindinger.
 Varme artikler
Varme artikler
-
 Gør renere, grønnere plast fra affaldsfiskdeleBrug af fiskeolie, forskere har lavet et polyurethan-lignende materiale. Kredit:Mikhailey Wheeler polyurethaner, en type plastik, er næsten overalt - i sko, tøj, køleskabe og byggematerialer. Men
Gør renere, grønnere plast fra affaldsfiskdeleBrug af fiskeolie, forskere har lavet et polyurethan-lignende materiale. Kredit:Mikhailey Wheeler polyurethaner, en type plastik, er næsten overalt - i sko, tøj, køleskabe og byggematerialer. Men -
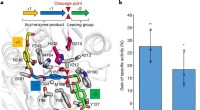 Konstrueret enzym i stand til at nedbryde PET på ti timeren, Strukturel model af 2-HE (MHET) 3 (farvet pindmodel) forankret i vildtype LCC (gråt bånd). Det formodede substratbindingssted for LCC kan opdeles i tre undersider (-2, −1, +1), hver i kontakt med
Konstrueret enzym i stand til at nedbryde PET på ti timeren, Strukturel model af 2-HE (MHET) 3 (farvet pindmodel) forankret i vildtype LCC (gråt bånd). Det formodede substratbindingssted for LCC kan opdeles i tre undersider (-2, −1, +1), hver i kontakt med -
 Undersøgelse viser, at enkelte atomer kan lave mere effektive katalysatorerForskere brugte en kombination af fire teknikker, repræsenteret her af fire indkommende stråler, at afsløre i hidtil uset detalje, hvordan et enkelt atom af iridium katalyserer en kemisk reaktion. Kre
Undersøgelse viser, at enkelte atomer kan lave mere effektive katalysatorerForskere brugte en kombination af fire teknikker, repræsenteret her af fire indkommende stråler, at afsløre i hidtil uset detalje, hvordan et enkelt atom af iridium katalyserer en kemisk reaktion. Kre -
 Ny sensor måler calciumkoncentrationer dybt inde i vævetCalciumbølger - en ny sensor konverterer lys til lyd for at visualisere calciumflux i kroppen. Kredit:B. van Rossum, G. Westmeyer / Münchens tekniske universitet Nøgleprocesser i kroppen styres af
Ny sensor måler calciumkoncentrationer dybt inde i vævetCalciumbølger - en ny sensor konverterer lys til lyd for at visualisere calciumflux i kroppen. Kredit:B. van Rossum, G. Westmeyer / Münchens tekniske universitet Nøgleprocesser i kroppen styres af
- Hvordan interagerer nervesystemet med andre systemer?
- Terningkast:Kvantemekanikforskere viser, at naturen er uforudsigelig
- Hvor meget forurener du din kontorluft blot ved at eksistere?
- Virusoverflader hjælper ingeniører med at studere vaccine- og genterapiapplikationer
- Sous vide tilberedningsmetode gør oksekødsprotein mere fordøjeligt
- Den franske hotelgigant AccorHotels køber Switzerlands Movenpick


