Hvordan adskiller elektronprikdiagrammerne af metalioner sig fra disse ikke -metale ioner?
metalioner:
* Tab af elektroner: Metalioner dannes ved at * miste * elektroner for at opnå en stabil elektronkonfiguration.
* positiv opladning: Tabet af elektroner resulterer i en positiv ladning på ion.
* færre prikker: Da elektroner går tabt, har metaliondiagrammer * færre * prikker end det neutrale atom.
* Eksempel: Natrium (NA) har 1 valenselektron. Når det danner Na+, mister det det elektron, hvilket resulterer i et diagram med * ingen * prikker.
ikke -metale ioner:
* Gevinst af elektroner: Ikke -metale ioner dannes ved at * vinde * elektroner for at opnå en stabil elektronkonfiguration.
* negativ opladning: Gevinsten af elektroner resulterer i en negativ ladning på ion.
* Flere prikker: Da elektroner opnås, har ikke -metal -iondiagrammer * flere * prikker end det neutrale atom.
* Eksempel: Chlor (CL) har 7 valenselektroner. Når det danner CL-, får det en elektron, hvilket resulterer i et diagram med * 8 * prikker.
Kortfattet:
* Metaller mister elektroner og bliver positive ioner med færre prikker.
* ikke -metaller får elektroner og bliver negative ioner med flere prikker.
Visuelt eksempel:
Lad os sammenligne natrium (metal) og klor (ikke -metal):
* na (neutral): Na • (1 prik)
* Na+ (ion): (Ingen prikker)
* cl (neutral): • Cl • • • • • (7 prikker)
* cl- (ion): • Cl • • • • • • • (8 prikker)
Sidste artikelHvad sker der med ammoniumchlorid, når de opvarmes?
Næste artikelHvordan opvarmes overfladen?
 Varme artikler
Varme artikler
-
 Ny forskning kan give bedre mad og hurtigere analyse af blodprøverAnne Bech Risum og Rasmus Bro ved siden af gaskromatografen på Institut for Fødevarevidenskab, ved Københavns Universitet (UCPH FOOD) i Danmark. Kredit:Morten Vormsborg Christiansen Gaskromatogr
Ny forskning kan give bedre mad og hurtigere analyse af blodprøverAnne Bech Risum og Rasmus Bro ved siden af gaskromatografen på Institut for Fødevarevidenskab, ved Københavns Universitet (UCPH FOOD) i Danmark. Kredit:Morten Vormsborg Christiansen Gaskromatogr -
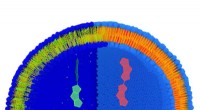 Måling af spændingen i en celle med et molekyleKunstnerens syn på en lipidmembran markeret med FliptR-molekylet. Lipiderne er blå (hydrofil del) og gule (hydrofob del). Når lipider strækkes (venstre del) har molekylet en kort levetid (grøn), hvori
Måling af spændingen i en celle med et molekyleKunstnerens syn på en lipidmembran markeret med FliptR-molekylet. Lipiderne er blå (hydrofil del) og gule (hydrofob del). Når lipider strækkes (venstre del) har molekylet en kort levetid (grøn), hvori -
 3-D-printede æggehvider overgår eksisterende fleksible elektronikmaterialerQiang Chang, førsteforfatter af æggehvidevæskerapporten med en prøve af æggehvidehydrogelen og væsken i Malcolm Xings laboratorium ved University of Manitoba. Kredit:Xing Enheder, der er fleksible
3-D-printede æggehvider overgår eksisterende fleksible elektronikmaterialerQiang Chang, førsteforfatter af æggehvidevæskerapporten med en prøve af æggehvidehydrogelen og væsken i Malcolm Xings laboratorium ved University of Manitoba. Kredit:Xing Enheder, der er fleksible -
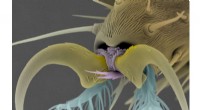 Lavpris, fluetrædepude-lignende klæbestruktur, der er i stand til gentagen fastgørelse/aftagningElektronmikrografi af fluefoden. De klæbende spatelformede setae (lyseblå strukturer) gør det muligt for fluen at sætte sig fast på genstande. Kredit:Hokkaido University of Education NIMS, HUE og
Lavpris, fluetrædepude-lignende klæbestruktur, der er i stand til gentagen fastgørelse/aftagningElektronmikrografi af fluefoden. De klæbende spatelformede setae (lyseblå strukturer) gør det muligt for fluen at sætte sig fast på genstande. Kredit:Hokkaido University of Education NIMS, HUE og


