Hvad er nyttige kemiske reaktioner?
1. Energiproduktion og opbevaring:
* forbrænding: Brændende brændstoffer som træ, kul, naturgas og benzin frigiver energi som varme og lys. Dette er grundlaget for kraftværker, køretøjer og mange varmesystemer.
* Fotosyntese: Planter bruger sollys til at omdanne kuldioxid og vand til glukose (sukker) og ilt. Denne reaktion brænder for plantevækst og er grundlaget for vores fødekæde.
* Elektrokemiske reaktioner i batterier: Batterier opbevarer energi ved at omdanne kemisk energi til elektrisk energi gennem oxidationsreduktionsreaktioner. Dette styrer alt fra mobiltelefoner til biler.
2. Materiel syntese og fremstilling:
* polymerisation: Deltagelse i små molekyler (monomerer) i lange kæder for at skabe polymerer som plast, gummi og fibre.
* haber-bosch-proces: Denne reaktion konverterer atmosfærisk nitrogen til ammoniak, en vigtig ingrediens til gødning, sprængstoffer og andre industrier.
* Produktion af farmaceutiske stoffer: Komplekse kemiske reaktioner bruges til at skabe medicin, vacciner og andre vigtige sundhedsprodukter.
* metalraffinering: Ekstraktion af metaller fra malm og deres forfining til anvendelige former involverer forskellige kemiske reaktioner.
3. Mad- og drikkevareproduktion:
* gæring: Mikrobiel omdannelse af kulhydrater til alkohol og kuldioxid, der bruges til brygning, vinfremstilling og brødbagning.
* Madlavning: Komplekse kemiske reaktioner forekommer, når mad opvarmes, hvilket ændrer dens smag, tekstur og ernæringsmæssigt indhold.
* Fødevarekonservering: Reaktioner som pickling, konserves og tørring ændrer miljøet, hvilket hæmmer ødelæggelsesmikrober.
4. Miljøbeskyttelse:
* Vandbehandling: Kemiske reaktioner bruges til at rense vand ved at fjerne forurenende stoffer som bakterier, tungmetaller og organiske forurenende stoffer.
* spildevandsbehandling: Spildevand behandles ved hjælp af reaktioner for at fjerne skadelige stoffer og nedbrydes organisk stof.
* Luftforureningskontrol: Reaktioner anvendes til at fjerne forurenende stoffer fra udstødningsgasser, såsom svovldioxid og nitrogenoxider.
5. Forskning og udvikling:
* Laboratoriesyntese: Kemikere udvikler konstant nye reaktioner for at skabe nye materialer, stoffer og andre produkter.
* Analytisk kemi: Reaktioner bruges i analytiske teknikker til at detektere og kvantificere stoffer, der hjælper med videnskabelig forskning og kvalitetskontrol.
Ud over disse kategorier bugner specifikke nyttige kemiske reaktioner:
* neutralisering: Syre-base-reaktioner bruges til at neutralisere skadelige stoffer og kontrollerer pH-niveauer.
* esterificering: Reaktioner, der producerer estere, der bruges i duftstoffer, smag og plast.
* Oxidationsreduktionsreaktioner: Disse er vigtige for mange processer, herunder respiration, korrosion og fotografering.
I sidste ende afhænger "anvendeligheden" af en kemisk reaktion af dens anvendelse. Mange tilsyneladende enkle reaktioner spiller afgørende roller i komplekse processer, hvilket gør dem uvurderlige for forskellige felter.
 Varme artikler
Varme artikler
-
 Flamme på! Hvordan AI kan tæmme en kompleks materialeteknik og transformere fremstillingJoseph Libera og Anthony Stark forbereder sig til in-situ Raman-spektroskopi. Kredit:Argonne National Laboratory Oprettelse af nanomaterialer med flammespraypyrolyse er kompleks, men forskere ved
Flamme på! Hvordan AI kan tæmme en kompleks materialeteknik og transformere fremstillingJoseph Libera og Anthony Stark forbereder sig til in-situ Raman-spektroskopi. Kredit:Argonne National Laboratory Oprettelse af nanomaterialer med flammespraypyrolyse er kompleks, men forskere ved -
 Forskning peger på en anden chance for afvist antibiotikakandidatKredit:University of Leeds En antibiotikakandidatforbindelse, der blev lagt på hylden i 1970erne til fordel for mere lovende lægemidler, kunne være et ekstra kig værd, ny forskning har fundet. St
Forskning peger på en anden chance for afvist antibiotikakandidatKredit:University of Leeds En antibiotikakandidatforbindelse, der blev lagt på hylden i 1970erne til fordel for mere lovende lægemidler, kunne være et ekstra kig værd, ny forskning har fundet. St -
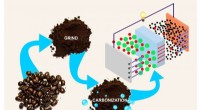 Kemikere syntetiserer elektroder til akkumulatorer fra kaffegrumsKredit:Natalia Deryugina En kemiker fra RUDN foreslog en billig og miljøvenlig måde at fremstille elektroder til lithium-ion-batterier fra kaffeproduktionsaffald. En artikel, der beskriver denne u
Kemikere syntetiserer elektroder til akkumulatorer fra kaffegrumsKredit:Natalia Deryugina En kemiker fra RUDN foreslog en billig og miljøvenlig måde at fremstille elektroder til lithium-ion-batterier fra kaffeproduktionsaffald. En artikel, der beskriver denne u -
 Nye værktøjer til at karakterisere biofilms fysiske egenskaberFigur (a) og (b) viser fluorescens- og oxygenkoncentrationskortet for henholdsvis en bakteriemikrokoloni. Figur (c) viser linjeprofilen af fluorescens (cirkler) og oxygenkoncentration (trekanter) la
Nye værktøjer til at karakterisere biofilms fysiske egenskaberFigur (a) og (b) viser fluorescens- og oxygenkoncentrationskortet for henholdsvis en bakteriemikrokoloni. Figur (c) viser linjeprofilen af fluorescens (cirkler) og oxygenkoncentration (trekanter) la
- Hvilken type geologiske træk dannes, hvor to kontinentale plader Collide forklarer?
- Monsunregn regner i indias finansielle kapital
- Har moderne videnskab en specifik forklaring på energien af energi?
- Hvad betyder graavitationsenergi?
- Hvorfor sod kunne være nøglen til at levere lægemidler til kræftceller
- Ocean funktioner og ændringer i fortiden udforskes for at foregribe fremtidigt klima


