Når zink reagerer med sulfuircsyre, hvilken masse brint produceres fra 31,8 g zink?
1. Skriv den afbalancerede kemiske ligning:
Zn (S) + H₂so₄ (aq) → Znso₄ (aq) + h₂ (g)
2. Bestem den molære masse af zink (Zn):
Den molære masse af Zn er 65,38 g/mol.
3. Beregn mol af zink:
* Mol Zn =(Mass of Zn) / (Molær masse af Zn)
* Mol Zn =31,8 g / 65,38 g / mol
* Mol Zn ≈ 0,487 mol
4. Påfør molforholdet:
* Fra den afbalancerede ligning producerer 1 mol Zn 1 mol H₂.
5. Beregn mol af brint (H₂):
* Mol H₂ =mol Zn
* Mol H₂ ≈ 0,487 mol
6. Bestem den molære masse af brint (H₂):
* Den molære masse af H₂ er 2,016 g/mol.
7. Beregn massen af brint:
* Masse af H₂ =(mol H₂) * (Molær masse af H₂)
* Masse af H₂ ≈ 0,487 mol * 2,016 g/mol
* Masse af H₂ ≈ 0,982 g
Derfor produceres ca. 0,982 gram brint fra 31,8 gram zink.
Sidste artikelKontakt med oxider er et eksempel på denne type forvitring.?
Næste artikelHvad er nyttige kemiske reaktioner?
 Varme artikler
Varme artikler
-
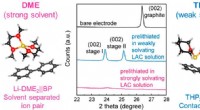 En innovativ proces forhindrer irreversibelt energitab i batterieren kemisk prelithieringsmetode til at maksimere ICE for blandingsanoderne ved hjælp af en reduktiv Li-arene kompleks løsning med reguleret solvationskraft, som gør det muligt for en fuld celle at udvi
En innovativ proces forhindrer irreversibelt energitab i batterieren kemisk prelithieringsmetode til at maksimere ICE for blandingsanoderne ved hjælp af en reduktiv Li-arene kompleks løsning med reguleret solvationskraft, som gør det muligt for en fuld celle at udvi -
 Ny indsigt i træning af højreaktive kemiske forbindelserDr. Jonas Warneke forklarer kemien bag meget reaktive molekyler, som forskes på Wilhelm Ostwald Instituttet. Kredit:Universität Leipzig Meget reaktive molekyler kan ikke overleve længe i naturen.
Ny indsigt i træning af højreaktive kemiske forbindelserDr. Jonas Warneke forklarer kemien bag meget reaktive molekyler, som forskes på Wilhelm Ostwald Instituttet. Kredit:Universität Leipzig Meget reaktive molekyler kan ikke overleve længe i naturen. -
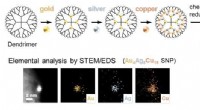 Sub-nanopartikelkatalysatorer fremstillet af møntelementer som effektive katalysatorerSkabelonsyntesen af møntmetallegerede SNPer ved hjælp af atomhybridiseringsmetoden. Tre metalelementer (guld, sølv, kobber) blandes her i en SNP på en en-nanometer skala. Kredit:Tokyo Institute of T
Sub-nanopartikelkatalysatorer fremstillet af møntelementer som effektive katalysatorerSkabelonsyntesen af møntmetallegerede SNPer ved hjælp af atomhybridiseringsmetoden. Tre metalelementer (guld, sølv, kobber) blandes her i en SNP på en en-nanometer skala. Kredit:Tokyo Institute of T -
 Nyt kunstigt enzym nedbryder sejt, træagtigt lignin:Undersøgelse viser løfte om at udvikle en ny …Woody lignin, set her i renset form, har et betydeligt løfte som et vedvarende biobrændstof, hvis det effektivt kan nedbrydes til nyttig form. Kredit:Andrea Starr | Pacific Northwest National Laborato
Nyt kunstigt enzym nedbryder sejt, træagtigt lignin:Undersøgelse viser løfte om at udvikle en ny …Woody lignin, set her i renset form, har et betydeligt løfte som et vedvarende biobrændstof, hvis det effektivt kan nedbrydes til nyttig form. Kredit:Andrea Starr | Pacific Northwest National Laborato
- Fremmedobjekt Oumuama var en naturlig krop, der besøgte fra et andet solsystem
- Succesfuld anvendelse af et miniaturiseret instrument til kuldioxid vertikale observationer
- Sådan finder du molekylære lim til effektivt at målrette sygdomme
- SAP mere ambitiøs efter kraftigt stigende overskud i 1. kvartal
- Europas nyhedsbureauer sprænger Google, Facebook for at plyndre indhold
- Egypten siger, at arkæologer har fundet flere artefakter ved udgravningen i Kairo


