Hvorfor er svovl et ikke -metal?
Fysiske egenskaber:
* sprød: Svovl er fast ved stuetemperatur og bryder let i små stykker.
* Dårlig leder af varme og elektricitet: Dette er et kendetegn for ikke -metaller.
* kedeligt udseende: Svovl har en gul farve og en pulveriseret struktur, i modsætning til det skinnende udseende af de fleste metaller.
Kemiske egenskaber:
* Lav elektronegativitet: Svovl har en relativt lav elektronegativitet sammenlignet med metaller. Dette betyder, at det har en svagere attraktion for elektroner.
* danner anioner (negativt ladede ioner): Svovl får let elektroner til at danne negativt ladede ioner, som sulfid (s 2- ). Dette er et typisk egenskab ved ikke -metaller.
* Formularer kovalente obligationer: Svovl danner kovalente bindinger med andre ikke -metaller, der deler elektroner til dannelse af molekyler som svovldioxid (så 2 ).
* reagerer med metaller for at danne sulfider: Svovl reagerer med metaller for at danne ioniske forbindelser kaldet sulfider. Dette er et kendetegn ved ikke -metaller, der interagerer med metaller.
Generelt udviser svovl flere egenskaber ved ikke -metaller end metaller, hvilket fører til dens klassificering som ikke -metal.
 Varme artikler
Varme artikler
-
 Dens elementære:Ultra-spordetektor tester guldrenhedKhadouja Harouaka (siddende) og Isaac Arnquist forbereder prøver i et ultrarent laboratorium, hvilket er nødvendigt for at sikre nøjagtige massespektrometrimålinger. Kredit:Andrea Starr | Pacific Nort
Dens elementære:Ultra-spordetektor tester guldrenhedKhadouja Harouaka (siddende) og Isaac Arnquist forbereder prøver i et ultrarent laboratorium, hvilket er nødvendigt for at sikre nøjagtige massespektrometrimålinger. Kredit:Andrea Starr | Pacific Nort -
 Et levende lys-lignende skær fra en fleksibel organisk LEDEn bøjelig organisk LED med en naturlig glimmerbagside frigiver en stærk, levende lys-lignende glød. Kredit:Andy Chen og Ambrose Chen Stearinlys giver en behagelig glød og sætter stemningen til en
Et levende lys-lignende skær fra en fleksibel organisk LEDEn bøjelig organisk LED med en naturlig glimmerbagside frigiver en stærk, levende lys-lignende glød. Kredit:Andy Chen og Ambrose Chen Stearinlys giver en behagelig glød og sætter stemningen til en -
 Forskere opfinder lette flydende metalmaterialerFigur 1. GB-eGaIn. Kredit:LIU Jing Flydende metal ved stuetemperatur, for eksempel Gallium-baseret legering, har høj elektrisk og termisk ledningsevne, og fremragende flydende. De kan bruges inden
Forskere opfinder lette flydende metalmaterialerFigur 1. GB-eGaIn. Kredit:LIU Jing Flydende metal ved stuetemperatur, for eksempel Gallium-baseret legering, har høj elektrisk og termisk ledningsevne, og fremragende flydende. De kan bruges inden -
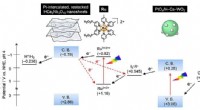 Ny fotokatalysator øger vandspaltningseffektiviteten til ren brintproduktionOxygenudviklingskatalysatoren reducerer effektivt koncentrationen af I3 - ioner og ændringer i hydrogenudviklingskatalysatoren forhindrer elektrontilbageførsel (stiplede røde linjer) og prioriterer
Ny fotokatalysator øger vandspaltningseffektiviteten til ren brintproduktionOxygenudviklingskatalysatoren reducerer effektivt koncentrationen af I3 - ioner og ændringer i hydrogenudviklingskatalysatoren forhindrer elektrontilbageførsel (stiplede røde linjer) og prioriterer
- Kan vi begrænse den globale opvarmning til 1,5 grader C?
- Ny bog:Underholdningsmedier former vores politik mere, end vi ved
- Mercurys 400 C-varme kan hjælpe den til at lave sin egen is
- Denne populære type investeringsfond taber næsten altid penge
- ALMA opløser gas påvirket af unge jetfly fra supermassive sorte hul
- Et objekt har en masse på 180 kg på månen Hvad er kraftgravet fungerende måne?


