Hvordan adskiller opløsninger sig fra forbindelser?
Løsninger
* Definition: En homogen blanding af to eller flere stoffer.
* sammensætning: Stofferne i en løsning bevarer deres individuelle egenskaber. Komponenterne kan adskilles med fysiske midler (som fordampning, filtrering osv.).
* dannelse: Opløsninger dannes gennem processen med opløsning, hvor et stof (opløste) opløses til et andet (opløsningsmidlet).
* Eksempler: Saltvand (salt opløst i vand), luft (gasser opløst i andre gasser), sukker opløst i vand.
Forbindelser
* Definition: Et rent stof dannet, når to eller flere forskellige elementer kemisk kombineres i et fast forhold.
* sammensætning: Elementerne i en forbindelse mister deres originale egenskaber og danner et nyt stof med unikke egenskaber.
* dannelse: Forbindelser dannes gennem kemiske reaktioner, hvilket resulterer i dannelse af nye kemiske bindinger.
* Eksempler: Vand (H₂O), kuldioxid (CO₂), natriumchlorid (NaCl).
Nøgleforskelle
* Kemiske bindinger: Forbindelser dannes gennem oprettelse af kemiske bindinger mellem elementer. Løsninger involverer ikke dannelsen af nye kemiske bindinger.
* fast forhold: Forbindelser har altid et fast forhold mellem elementer. Løsninger kan have forskellige koncentrationer af det opløste stof.
* adskillelse: Forbindelser kan kun adskilles med kemiske midler (f.eks. Elektrolyse). Løsninger kan adskilles med fysiske midler.
* egenskaber: Forbindelser har unikke egenskaber, der er forskellige fra de elementer, de er lavet af. Løsninger bevarer egenskaberne for de individuelle komponenter.
Analogi:
Tænk på det sådan:Forestil dig at lave en salat.
* Løsning: Den påklædning, du bruger, er en løsning. Det er en blanding af olie og eddike, men hver ingrediens bevarer stadig sine egenskaber.
* Forbindelse: Salat i din salat er en forbindelse. Det er lavet af forskellige elementer, der har kombineret kemisk for at danne et nyt stof med forskellige egenskaber fra disse elementer alene.
 Varme artikler
Varme artikler
-
 Insekter i frysende områder har et protein, der fungerer som frostvæskeFrostvæskeproteiner er en unik klasse af proteiner, hvis virkemekanisme ikke er forstået. Dette kunstneriske indtryk viser brugen af sum-frekvensgenereringsspektroskopi til at bestemme proteinernes
Insekter i frysende områder har et protein, der fungerer som frostvæskeFrostvæskeproteiner er en unik klasse af proteiner, hvis virkemekanisme ikke er forstået. Dette kunstneriske indtryk viser brugen af sum-frekvensgenereringsspektroskopi til at bestemme proteinernes -
 Ikke-klorerede opløsningsmiddelbehandlede højtydende ambipolære transistorer(a) PITTI-BTs molekylære struktur. (b) Fotografi af PITTI-BT-film. (c) P-xylenopløsning af PITTI-BT. AFM-billeder af polymerfilmene fremstillet af (d, g) on-center og (e, f, h, i) off-center SC-metode
Ikke-klorerede opløsningsmiddelbehandlede højtydende ambipolære transistorer(a) PITTI-BTs molekylære struktur. (b) Fotografi af PITTI-BT-film. (c) P-xylenopløsning af PITTI-BT. AFM-billeder af polymerfilmene fremstillet af (d, g) on-center og (e, f, h, i) off-center SC-metode -
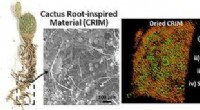 Kaktusrødder inspirerer til skabelse af vandfastholdende materialeKredit:American Chemical Society Under sjældne ørkenregn, kaktusser spilder ingen tid med at suge op og gemme en storms dyrebare nedbør. Inspireret af dette naturfænomen, videnskabsmænd rapportere
Kaktusrødder inspirerer til skabelse af vandfastholdende materialeKredit:American Chemical Society Under sjældne ørkenregn, kaktusser spilder ingen tid med at suge op og gemme en storms dyrebare nedbør. Inspireret af dette naturfænomen, videnskabsmænd rapportere -
 Bærende sammenfiltringer i polymerglasBlandede homopolymer tynde film. Makroskopisk eksperimentel hundebenformet prøve (billedet) indlæst i TUTTUT for enaksial forlængelse. Molekylære simuleringer skildrer kæder, der glider forbi hinanden
Bærende sammenfiltringer i polymerglasBlandede homopolymer tynde film. Makroskopisk eksperimentel hundebenformet prøve (billedet) indlæst i TUTTUT for enaksial forlængelse. Molekylære simuleringer skildrer kæder, der glider forbi hinanden
- Hvad var Albert Einsteins Epiphany?
- Hvad er den kemiske ligning for pyrogallsyre og natriumhydroxid?
- Amazon planlægger en ny købmandsbutik i L.A., da den tænker over, hvordan man erobrer branchen
- Hvilket trin i cellecyklus er mest aktiv med hensyn til genhandling?
- Marine mikrofibre:mindre plastik end forudsagt
- At lægge vægt på social leg i børnehaven forbedrer det akademiske, reducerer lærernes udbrændt…


