Hvad er den generelle form for en enkeltudskiftningsreaktion?
A + BC → AC + B
hvor:
* a er et mere reaktivt element eller ion
* b er et mindre reaktivt element eller ion
* C er et element eller ion
Dette betyder, at et mere reaktivt element eller ion (A) fortrænger et mindre reaktivt element eller ion (B) fra en forbindelse (BC).
nøglepunkter at huske:
* Enkeltudskiftningsreaktioner involverer udskiftning af et element i en forbindelse med et andet element.
* Reaktiviteten af de involverede elementer bestemmer, om en enkeltudskiftningsreaktion vil forekomme.
* Reaktionen fortsætter kun, hvis det mere reaktive element kan fortrænge det mindre reaktive element.
Eksempler på reaktioner med en enkelt erstatning:
* zn + cuso 4 → Znso 4 + Cu (Zink er mere reaktiv end kobber)
* 2na + 2H 2 O → 2naoh + h 2 (Natrium er mere reaktiv end brint)
* fe + cucl 2 → FECL 2 + Cu (Jern er mere reaktivt end kobber)
 Varme artikler
Varme artikler
-
 Molekyle egenskaber ændres gennem lysTobias Thomanek, Enrique Mendez Vega og Wolfram Sander (fra venstre). Ikke afbildet, men væsentligt involveret i undersøgelsen:Iris Trosien. Kredit:RUB, Marquard Inden for computerteknik, magnetis
Molekyle egenskaber ændres gennem lysTobias Thomanek, Enrique Mendez Vega og Wolfram Sander (fra venstre). Ikke afbildet, men væsentligt involveret i undersøgelsen:Iris Trosien. Kredit:RUB, Marquard Inden for computerteknik, magnetis -
 Fremstilling af brintlagermaterialer fra industriaffaldKredit:Pixabay/CC0 Public Domain Uanset om det er biler, energi eller mobiltelefoner, er det moderne samfund bygget på metaller, og vores fremtid afhænger også stærkt af disse materialer. At opbeva
Fremstilling af brintlagermaterialer fra industriaffaldKredit:Pixabay/CC0 Public Domain Uanset om det er biler, energi eller mobiltelefoner, er det moderne samfund bygget på metaller, og vores fremtid afhænger også stærkt af disse materialer. At opbeva -
 Forskere bygger robotforsker, der allerede har opdaget en ny katalysatorMobil robotforsker læsser et stativ med eksperimentelle prøver. Kredit:University of Liverpool Forskere ved University of Liverpool har bygget en intelligent mobil robotforsker, der kan arbejde 24
Forskere bygger robotforsker, der allerede har opdaget en ny katalysatorMobil robotforsker læsser et stativ med eksperimentelle prøver. Kredit:University of Liverpool Forskere ved University of Liverpool har bygget en intelligent mobil robotforsker, der kan arbejde 24 -
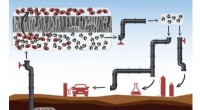 Mere effektiv adskillelse af metan og CO2Naturgas eller biogas skal altid renses før brug. Først, metanmolekylerne (i sort og hvid) er adskilt fra CO 2 molekyler (i rødt og sort) ved hjælp af membraner med bittesmå porer, hvorigennem kun C
Mere effektiv adskillelse af metan og CO2Naturgas eller biogas skal altid renses før brug. Først, metanmolekylerne (i sort og hvid) er adskilt fra CO 2 molekyler (i rødt og sort) ved hjælp af membraner med bittesmå porer, hvorigennem kun C
- Du slipper en sten i damskripler bevæger sig væk fra det punkt, hvor de indtastede vand, når de b…
- Hvem kæmpede i de gamle græske slag ved Himera? Kemiske beviser giver svar
- Hvordan ord betyder noget, når man står over for problemet med børn i pleje
- Hvad sker der, når Moon drejer sig om solen?
- Hvor meget betyder en videnskabstekstbog?
- Er nanosølv giftigt?


