Hvilken type krystal består positive metalkationer omgivet af valenselektroner, der doneres atomerne og hører til som en helhed?
* positive metalkationer: I metalliske krystaller mister metalatomerne deres valenselektroner og danner positivt ladede ioner (kationer).
* Elektronhav: Disse mistede elektroner hører ikke til noget specifikt atom, men danner snarere et "hav" af delokaliserede elektroner, der bevæger sig frit gennem hele krystalstrukturen.
* stærk metallisk binding: Tiltrækningen mellem de positive kationer og havet af elektroner skaber stærk metallisk binding, som er ansvarlig for de karakteristiske egenskaber ved metaller som høj ledningsevne (både elektrisk og termisk), formbarhed og duktilitet.
Eksempler på metalliske krystaller: Jern, kobber, guld, sølv, aluminium og mange andre metaller danner denne type krystalstruktur.
 Varme artikler
Varme artikler
-
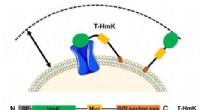 Zombie-scanning muliggør undersøgelse af peptid-receptor-interaktioner på celleoverfladenDet bundne toksin (T-HmK) trækkes fri og bindes til en kaliumkanal (blå) udtrykt i cellemembranen. Reaktionsvolumenet, som en T-HmK kan besøge (pil med to hoveder) bestemmes af de kombinerede længder
Zombie-scanning muliggør undersøgelse af peptid-receptor-interaktioner på celleoverfladenDet bundne toksin (T-HmK) trækkes fri og bindes til en kaliumkanal (blå) udtrykt i cellemembranen. Reaktionsvolumenet, som en T-HmK kan besøge (pil med to hoveder) bestemmes af de kombinerede længder -
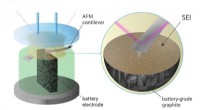 Forskere får et smugkig på en nøgleproces i batterilevetidenEn hovedoversigt over eksperimentet. Kredit:Pavel Odinev / Skoltech Forskere fra Skoltech Center for Energividenskab og Teknologi (CEST) visualiserede dannelsen af en fast elektrolyt-interfase p
Forskere får et smugkig på en nøgleproces i batterilevetidenEn hovedoversigt over eksperimentet. Kredit:Pavel Odinev / Skoltech Forskere fra Skoltech Center for Energividenskab og Teknologi (CEST) visualiserede dannelsen af en fast elektrolyt-interfase p -
 Bærbar biosensor advarer mod hjerteanfald og slagtilfældeDen bærbare måleenhed med USB -interface til tilslutning til bærbar computer. Softwaren installeret i bærbar computer giver GUI til at styre måleparametre og vise testresultaterne. Indsæt viser den em
Bærbar biosensor advarer mod hjerteanfald og slagtilfældeDen bærbare måleenhed med USB -interface til tilslutning til bærbar computer. Softwaren installeret i bærbar computer giver GUI til at styre måleparametre og vise testresultaterne. Indsæt viser den em -
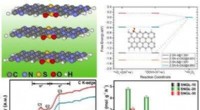 Forskere indser effektiv hydrogenperoxidproduktion i syreIllustration af forskningen. Kredit:Prof. Guans gruppe Som et af de 100 vigtigste kemikalier i verden er hydrogenperoxid (H2 O2 ) fremstilles hovedsageligt ved den energi- og affaldsintensive anthr
Forskere indser effektiv hydrogenperoxidproduktion i syreIllustration af forskningen. Kredit:Prof. Guans gruppe Som et af de 100 vigtigste kemikalier i verden er hydrogenperoxid (H2 O2 ) fremstilles hovedsageligt ved den energi- og affaldsintensive anthr
- Hvor stor er størrelsen på solen?
- Astronomer opdager en mørk fortid for planet-spiser Death Star
- Indeholder solen mere brint eller helium?
- Hvor mange gram fluor skal der til for at reagere med 6,20 g fosfor?
- Forskning forbedrer ydeevnen af Tysklands nye fusionsenhed
- Hvilket begreb om evolution forklarer, hvorfor organismer er konstrueret til at imødekomme de krav,…


