Hvor mange mol sølvnitrat ville være påkrævet for at reagere med 2,00 natriumphosphat?
1. Skriv den afbalancerede kemiske ligning:
3 Agno₃ (aq) + na₃po₄ (aq) → Ag₃po₄ (s) + 3 nano₃ (aq)
2. Bestem molforholdet fra den afbalancerede ligning:
Ligningen viser, at 3 mol sølvnitrat (Agno₃) reagerer med 1 mol natriumphosphat (Na₃po₄).
3. Beregn molen af sølvnitrat:
Da du har 2,00 mol natriumphosphat, har du brug for tre gange den mængde sølvnitrat:
Mol af agno₃ =2,00 mol na₃po₄ × (3 mol Agno₃ / 1 mol na₃po₄) = 6,00 mol Agno₃
Derfor har du brug for 6,00 mol sølvnitrat for at reagere med 2,00 mol natriumphosphat.
Sidste artikelHvad er nettoionisk ligning for aluminiumsbromid og sølvacetat?
Næste artikelHvad er arbejdsprincippet for opløst iltmåler?
 Varme artikler
Varme artikler
-
 Konstrueret insulin, der kan aktiveres af forhøjet blodsukker, kan forbedre diabetikernes livskvali…“[Glukose-responsiv insulin] har været et mangeårigt mål for diabetesområdet, ”Siger professor Michael Strano. Hvis det gøres korrekt, du kunne gøre det, så diabetikere lejlighedsvis kunne tage en dos
Konstrueret insulin, der kan aktiveres af forhøjet blodsukker, kan forbedre diabetikernes livskvali…“[Glukose-responsiv insulin] har været et mangeårigt mål for diabetesområdet, ”Siger professor Michael Strano. Hvis det gøres korrekt, du kunne gøre det, så diabetikere lejlighedsvis kunne tage en dos -
 Forskere finder en løsning til at måle skadelige plastikpartikler i menneskeligt spildevandDette billede er genereret af simple, en FTIR-partikelanalysesoftware, efter sammenligning af de erhvervede partikelspektre med en referencedatabase. Kredit:University of Portsmouth Forskere er ko
Forskere finder en løsning til at måle skadelige plastikpartikler i menneskeligt spildevandDette billede er genereret af simple, en FTIR-partikelanalysesoftware, efter sammenligning af de erhvervede partikelspektre med en referencedatabase. Kredit:University of Portsmouth Forskere er ko -
 Forskere udvikler bioniske blade til distribueret landbrugKelsey Sakimoto, postdoc ved Center for Miljø, udforsker, hvordan man bruger solen til at berige jorden med et kunstigt blad og konstruerede bakterier. Kredit:Rose Lincoln/Harvard Staff Photographer
Forskere udvikler bioniske blade til distribueret landbrugKelsey Sakimoto, postdoc ved Center for Miljø, udforsker, hvordan man bruger solen til at berige jorden med et kunstigt blad og konstruerede bakterier. Kredit:Rose Lincoln/Harvard Staff Photographer -
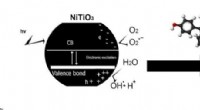 Kemikere omdanner titanium nanopartikler til et effektivt våben mod forureningDen nye metode Kredit:Yahya Absalan Forskere fra RUDN University (Rusland) har fundet frem til en ny metode til at omdanne titanium nanopartikler til et effektivt stof, der er i stand til at fjern
Kemikere omdanner titanium nanopartikler til et effektivt våben mod forureningDen nye metode Kredit:Yahya Absalan Forskere fra RUDN University (Rusland) har fundet frem til en ny metode til at omdanne titanium nanopartikler til et effektivt stof, der er i stand til at fjern
- ALMAs evne til at se et kosmisk hul bekræftet
- I verdens hovedstad for vaniljeproduktion, næsten tre ud af fire landmænd siger, at de ikke har no…
- Hvilken celledel inde i en amøbe bruges højst sandsynligt til at lave forlængelsen?
- Når kontinenter støder sammen:Rekonstruering af dannelsen af det Himalaya-Tibetanske Plateau
- Hvad er det største atom mellem carbonbor lithium og fluor?
- At arbejde hjemmefra under COVID-19:Hvad ønsker medarbejderne virkelig?


