Hvor mange yderligere valenselektroner har chlor brug for at have en fuld skal?
Her er hvorfor:
* Elektronkonfiguration: Klor har 17 elektroner. Dens elektronkonfiguration er 2, 8, 7. Dette betyder, at den har 7 elektroner i sin yderste skal (Valence Shell).
* octet regel: Atomer har en tendens til at vinde, tabe eller dele elektroner for at opnå en stabil konfiguration af 8 elektroner i deres yderste skal (oktetreglen).
* Fuld skal: For at opnå en fuld skal, har klor brug for endnu en elektron for at få sin valensskal til at have 8 elektroner.
Sidste artikelHvorfor kan klor kun acceptere en elektron?
Næste artikelHvordan vil natrium og klor blive stabile?
 Varme artikler
Varme artikler
-
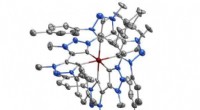 Moderne alkymi skaber selvlysende jernmolekylerKredit:Lunds Universitet En gruppe forskere ved Lunds Universitet i Sverige har lavet det første jernbaserede molekyle, der er i stand til at udsende lys. Dette kunne bidrage til udviklingen af
Moderne alkymi skaber selvlysende jernmolekylerKredit:Lunds Universitet En gruppe forskere ved Lunds Universitet i Sverige har lavet det første jernbaserede molekyle, der er i stand til at udsende lys. Dette kunne bidrage til udviklingen af -
 Strukturelle farver, uden glimmerDenne legetøjsdinosaur blev malet med en ny type ikke-iriserende strukturel farve. Kredit:Dongpeng Yang Strukturelle farver, som dem, der findes i nogle sommerfugles vinger, fugles fjer og billers
Strukturelle farver, uden glimmerDenne legetøjsdinosaur blev malet med en ny type ikke-iriserende strukturel farve. Kredit:Dongpeng Yang Strukturelle farver, som dem, der findes i nogle sommerfugles vinger, fugles fjer og billers -
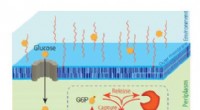 Opdagelse af nyt fænomen en game-changer for effektiv bioproduktion af nyttige kemikalierG6P-sekretionsmekanismen opdaget i denne undersøgelse. Kredit:Kobe University Et forskningssamarbejde har opdaget en ny mekanisme, hvorved glukose, der blev fanget af E. coli, derefter udskilles fr
Opdagelse af nyt fænomen en game-changer for effektiv bioproduktion af nyttige kemikalierG6P-sekretionsmekanismen opdaget i denne undersøgelse. Kredit:Kobe University Et forskningssamarbejde har opdaget en ny mekanisme, hvorved glukose, der blev fanget af E. coli, derefter udskilles fr -
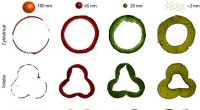 Fluorescerende alkometer gør optimering af katalysatorer meget nemmereFluorescensmikroskopibilleder viser virkningerne af forskellige former på katalysatoraktivitet. Kredit:Utrecht University En ny test for industrielle katalysatorer udviklet af kemikere ved Utrecht
Fluorescerende alkometer gør optimering af katalysatorer meget nemmereFluorescensmikroskopibilleder viser virkningerne af forskellige former på katalysatoraktivitet. Kredit:Utrecht University En ny test for industrielle katalysatorer udviklet af kemikere ved Utrecht
- Driver massive galakseudstrømninger med supermassive sorte huller
- Fyrre-seks transistorer konstrueret på seks CNT'er er den mest komplicerede enhed af sin art til da…
- Hvad er atmosfæren på alle planeter lavet af?
- Hvor meget vejer en kvart på halvdelen og vejer?
- Hvordan er mængden af elektrisk energi anvendt sammenlignet med lys produceret?
- Molekylær knude vinder rekord for verdens strammeste


