Hvad er nogen forbindelse, der øger antallet af hydroxidioner, når de opløses i vand?
Her er en sammenbrud:
* hydroxidioner (OH-) er negativt ladede ioner, der er karakteristiske for alkaliske (grundlæggende) løsninger.
* baser er stoffer, der, når de opløses i vand, producerer hydroxidioner. Dette øger opløsningens pH, hvilket gør den mere alkalisk.
Eksempler på baser:
* natriumhydroxid (NaOH): En stærk base, der fuldstændigt adskiller sig i vand for at danne natriumioner (Na+) og hydroxidioner (OH-).
* calciumhydroxid (CA (OH) 2): En stærk base, der også adskiller sig fuldt ud i vand.
* ammoniak (NH3): En svag base, der reagerer med vand til dannelse af ammoniumioner (NH4+) og hydroxidioner (OH-).
Vigtig note: Udtrykkene "base" og "alkali" bruges undertiden om hverandre, men teknisk henviser en alkali specifikt til en base, der opløses i vand. I de fleste sammenhænge anvendes de to udtryk synonymt.
 Varme artikler
Varme artikler
-
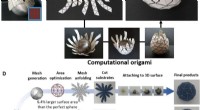 Computational origami:En universel metode til at indpakke 3-D buede overflader med ikke-strækbare m…Reverse engineering computerorigami til konform indpakning. (A) Rynker dannes ved tæt indpakning af et rektangulært ark papir omkring en ikke -nul Gauss -overflade. (B) Fraktale snitmønstre kan undgå
Computational origami:En universel metode til at indpakke 3-D buede overflader med ikke-strækbare m…Reverse engineering computerorigami til konform indpakning. (A) Rynker dannes ved tæt indpakning af et rektangulært ark papir omkring en ikke -nul Gauss -overflade. (B) Fraktale snitmønstre kan undgå -
 Ny reaktion kan udløse en alternativ tilgang til ammoniakproduktionAberrationskorrigerede scanningstransmissionselektronmikroskopi (STEM) billeder af CNSer. (A) De uberørte nanospikes udviser lag af foldet grafen med en vis strukturel lidelse på grund af nitrogeninda
Ny reaktion kan udløse en alternativ tilgang til ammoniakproduktionAberrationskorrigerede scanningstransmissionselektronmikroskopi (STEM) billeder af CNSer. (A) De uberørte nanospikes udviser lag af foldet grafen med en vis strukturel lidelse på grund af nitrogeninda -
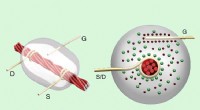 Ingeniører laver transistorer og elektroniske enheder udelukkende af trådTop- og tværsnitsbilleder af gevindbaseret transistor. Kilde (S) og afløbsledninger (D) er bundet til carbon nanorør belagt tråd, dyppet i en elektrolytisk gate gel. En gateledning er forbundet til ge
Ingeniører laver transistorer og elektroniske enheder udelukkende af trådTop- og tværsnitsbilleder af gevindbaseret transistor. Kilde (S) og afløbsledninger (D) er bundet til carbon nanorør belagt tråd, dyppet i en elektrolytisk gate gel. En gateledning er forbundet til ge -
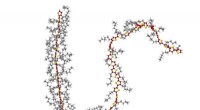 Forskere opdager en måde at kontrollere farven på OLED'erTil venstre, en polymer med en aflang rygrad (rød-gul). De lange sidekæder (grå) af de molekylære byggesten danner et stillads, der stabiliserer forlængelsen. Til højre, en polymer med en bøjet rygrad
Forskere opdager en måde at kontrollere farven på OLED'erTil venstre, en polymer med en aflang rygrad (rød-gul). De lange sidekæder (grå) af de molekylære byggesten danner et stillads, der stabiliserer forlængelsen. Til højre, en polymer med en bøjet rygrad
- Hvordan påvirker vanddamp miljøet?
- Hvilket udstyr vil du bruge til at måle strømmen i et kredsløb?
- Hvilke organisationer tager fejl af afbrydelser på arbejdet
- Første visning af brint ved metal-til-metalhydrid-grænsefladen
- En stor ting:Florida står klar til orkanen Dorian
- I hvilken del af solen skabes energi?


