Et nitrogenmolekyle reagerer med tre hydrogenmolekyler for at producere to ammoniak, der hver indeholder et og atomer?
* reaktanterne:
* nitrogen (n₂): Et diatomisk molekyle, hvilket betyder, at det har to nitrogenatomer bundet sammen.
* brint (H₂): Også et diatomisk molekyle med to hydrogenatomer bundet sammen.
* Produktet:
* ammoniak (NH₃): Et molekyle indeholdende et nitrogenatom og tre hydrogenatomer.
Den afbalancerede kemiske ligning:
Reaktionen kan repræsenteres ved følgende afbalancerede kemiske ligning:
N₂ + 3H₂ → 2NH₃
hvad ligningen fortæller os:
* Et molekyle af nitrogen (N₂) reagerer med tre molekyler brint (3H₂) for at producere to molekyler af ammoniak (2NH₃).
* atomerne er konserveret: Bemærk, at der er to nitrogenatomer (N) på begge sider af ligningen og seks hydrogenatomer (H) på begge sider. Dette sikrer, at reaktionen adlyder loven om bevarelse af masse.
Betydningen af Haber-Bosch-processen:
Haber-Bosch-processen er utroligt vigtig, fordi den producerer ammoniak, som er en nøgleingrediens i:
* Gødning: Ammoniak er grundlaget for de fleste nitrogenholdige gødning, som er vigtige for plantevækst.
* eksplosiver: Ammoniak bruges til at producere eksplosiver som ammoniumnitrat.
* Andre industrielle anvendelser: Ammoniak bruges i forskellige industrielle processer, herunder produktion af plast, tekstiler og lægemidler.
Sidste artikelHvad er kobberchlor?
Næste artikelHvor mange atomer er der i 1,3 x 1022 molekyler af NO2?
 Varme artikler
Varme artikler
-
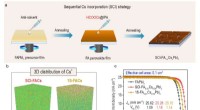 Afkoblingsteknik af formamidinium-cæsiumperovskiter til effektive solceller(a) Skematisk diagram af SCI-FA1-xCsxPbI3 perovskitfilm fremstillet ved afkobling af krystallisationsprocessen af formamidinium og cæsium. (b) 3D distribution af Cs+ i SCI-FA0,91 Cs0.09 PbI3 og 1S-F
Afkoblingsteknik af formamidinium-cæsiumperovskiter til effektive solceller(a) Skematisk diagram af SCI-FA1-xCsxPbI3 perovskitfilm fremstillet ved afkobling af krystallisationsprocessen af formamidinium og cæsium. (b) 3D distribution af Cs+ i SCI-FA0,91 Cs0.09 PbI3 og 1S-F -
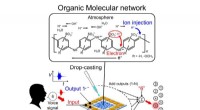 Intelligens, der kommer fra tilfældige polymernetværkStemmegenkendelse ved hjælp af sulfoneret polyanilin. Kredit:Creative Commons CC-BY, kredit:2021, Yuki Usami et al., Avancerede materialer Reservoir computing (RC) tackler komplekse problemer ved
Intelligens, der kommer fra tilfældige polymernetværkStemmegenkendelse ved hjælp af sulfoneret polyanilin. Kredit:Creative Commons CC-BY, kredit:2021, Yuki Usami et al., Avancerede materialer Reservoir computing (RC) tackler komplekse problemer ved -
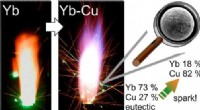 Forskere bruger sjældne jordarters metaller i legeringspulvere til at producere grønne, iøjnefald…Grafisk abstrakt. Kredit:ACS Omega (2022). DOI:10.1021/acsomega.2c03081 Stjernekastere kan være meget sjove - glimtende, brusende og spyttede lysbuer ud fra håndholdte pinde eller rør på jorden. Me
Forskere bruger sjældne jordarters metaller i legeringspulvere til at producere grønne, iøjnefald…Grafisk abstrakt. Kredit:ACS Omega (2022). DOI:10.1021/acsomega.2c03081 Stjernekastere kan være meget sjove - glimtende, brusende og spyttede lysbuer ud fra håndholdte pinde eller rør på jorden. Me -
 Ny undersøgelse analyserer levedygtigheden af bæredygtige brændstoffer udviklet gennem ny proce…En pilotreaktor, udviklet af Vertimass og placeret hos TechnipFMC, kan opskalere processen, der omdanner ethanol til brændstof, der er egnet til luftfart, forsendelse og andre tunge applikationer. Kre
Ny undersøgelse analyserer levedygtigheden af bæredygtige brændstoffer udviklet gennem ny proce…En pilotreaktor, udviklet af Vertimass og placeret hos TechnipFMC, kan opskalere processen, der omdanner ethanol til brændstof, der er egnet til luftfart, forsendelse og andre tunge applikationer. Kre
- PE, PP og PS:Den mest udbredte type mikroplast i Middelhavets kystnære farvande
- Under anafase af meiose har kromosomerne en eller to kromatider, når de bevæger sig mod poler?
- I en F2 -generation havde kun mandlige frugter, der havde hvide øjne, hvad hedder dette arvemønste…
- Det kan være svært for offentligheden at tolke orkanprognoser
- Næsten atomisk fladt silicium kan være med til at bane vejen for nye kemiske sensorer
- Sæt ubrugt og doven jord til at arbejde for at lette krisen med økonomisk overkommelige boliger


