Hvordan finder du normalitet af jernholdigt ammoniumsulfat?
Forståelse af normalitet
* Normalitet (n) er et mål for koncentration, der henviser til antallet af gramækvivalenter af et opløst stof opløst pr. Liter opløsning.
* Gram ækvivalent vægt (GEW) er molekylvægten af et stof divideret med antallet af ækvivalenter, det producerer i en reaktion.
trin for at bestemme normalitet
1. Skriv den afbalancerede kemiske ligning: Dette er afgørende for at bestemme antallet af ækvivalenter, det jernholdige ammoniumsulfat vil producere i en specifik reaktion. Lad os for eksempel antage, at du bruger det som et reduktionsmiddel i en redoxreaktion, hvor fe²⁺ oxideres til fe³⁺:
Fe²⁺ + e⁻ → fe³⁺
2. Beregn molekylvægten (MW) af jernholdigt ammoniumsulfat (Feso₄ (NH₄) ₂SO₄ · 6H₂O):
* FE:55,845 g/mol
* S:32,065 g/mol
* O:15.999 g/mol
* N:14,007 g/mol
* H:1,008 g/mol
*MW =(55.845 + 32.065 + 15.999*4 + 14.007*2 + 1,008*8 + 15.999*6) =392.14 g/mol
3. Bestem antallet af ækvivalenter: I reaktionen ovenfor producerer en mol af jernholdigt ammoniumsulfat (feso₄ (NH₄) ₂SO₄ · 6H₂O) en mol Fe²⁺, der frigiver en elektron (E⁻). Derfor svarer en mol af jernholdigt ammoniumsulfat til et ækvivalent.
4. Beregn gramækvivalentvægten (GEW):
* GEW =MW / antal ækvivalenter =392,14 g / mol / 1 =392,14 g / ækvivalent
5. Bestem massen af jernholdigt ammoniumsulfat: Vej den nøjagtige masse af jernholdigt ammoniumsulfat, du bruger til din løsning.
6. Beregn normaliteten:
* Normalitet (n) =(masse af opløst
Eksempel:
* Du opløser 10,0 g jernholdigt ammoniumsulfat i 250 ml vand.
* Trin 1: Du har den afbalancerede ligning fra tidligere.
* Trin 2: Du beregnet MW til at være 392,14 g/mol.
* Trin 3: Du ved, at en muldvarp producerer en ækvivalent.
* Trin 4: Du beregnet GEW til at være 392,14 g/tilsvarende.
* Trin 5: Du har 10,0 g jernholdigt ammoniumsulfat.
* Trin 6:
* N =(10,0 g / 392,14 g / ækvivalent) / (0,250 L)
* N ≈ 0,102 n
Vigtige noter:
* Hydreret salt: Sørg for at bruge molekylvægten af den hydratiserede form af jernholdigt ammoniumsulfat (feso₄ (NH₄) ₂SO₄ · 6H₂O), hvis du bruger det hydratiserede salt.
* reaktionsspecifik: Normalitet er reaktionsspecifik. Antallet af ækvivalenter varierer afhængigt af reaktionen, hvor det jernholdige ammoniumsulfat anvendes.
* renhed: Hvis dit jernholdige ammoniumsulfat ikke er 100% rent, skal du justere dine beregninger i overensstemmelse hermed.
Sidste artikelNår en ionisk forbindelse opløses i vand, danner dets klart?
Næste artikelHvilke kemiske elementer er i farveblyanter?
 Varme artikler
Varme artikler
-
 Ingeniører bruger Tiki fakler til undersøgelse af sod, diesel filtrePrøvekerner fra partikelfiltre, der bruges til test. Kredit:University of Notre Dame Kemiske ingeniører testmetoder til forbedring af dieselmotorers effektivitet og samtidig opretholde ydeevnen få
Ingeniører bruger Tiki fakler til undersøgelse af sod, diesel filtrePrøvekerner fra partikelfiltre, der bruges til test. Kredit:University of Notre Dame Kemiske ingeniører testmetoder til forbedring af dieselmotorers effektivitet og samtidig opretholde ydeevnen få -
 Nye superkondensatorer lagrer elektrisk ladning i tekstilmaterialerKredit:Asociacion RUVID Forskere fra Alcoi campus ved Valencias Polytekniske Universitet (UPV) har udviklet nye enheder, der lagrer elektrisk ladning i tekstilmaterialer, som kunne bruges til, for
Nye superkondensatorer lagrer elektrisk ladning i tekstilmaterialerKredit:Asociacion RUVID Forskere fra Alcoi campus ved Valencias Polytekniske Universitet (UPV) har udviklet nye enheder, der lagrer elektrisk ladning i tekstilmaterialer, som kunne bruges til, for -
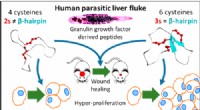 Et molekyle produceret af en thailandsk leverparasit kan være løsningen på de ikke-helende sårKredit:ACS Hver dag amputeres 12 australske diabetikere på grund af et sår, der ikke heler. Globalt set det er en hvert 30. sekund. Et molekyle produceret af en thailandsk leverparasit kan være l
Et molekyle produceret af en thailandsk leverparasit kan være løsningen på de ikke-helende sårKredit:ACS Hver dag amputeres 12 australske diabetikere på grund af et sår, der ikke heler. Globalt set det er en hvert 30. sekund. Et molekyle produceret af en thailandsk leverparasit kan være l -
 Skift af spor:Vende elektronernes kurs gennem naturens solcellerKredit:CC0 Public Domain Tænk på et tog, der kommer ned ad skinnerne til et skiftepunkt, hvor det kunne køre enten til højre eller venstre - og det kører altid til højre. Fotosyntetiske organisme
Skift af spor:Vende elektronernes kurs gennem naturens solcellerKredit:CC0 Public Domain Tænk på et tog, der kommer ned ad skinnerne til et skiftepunkt, hvor det kunne køre enten til højre eller venstre - og det kører altid til højre. Fotosyntetiske organisme
- Er babyboomere på vej tilbage til religion?
- Intensiteten af stolthed folk føler for en given handling eller egenskab er sat af et implicit me…
- Beskriv, hvordan videnskaben unikt udføres af mennesker?
- Vægt af produceret vand pr. Gallon?
- Drikkevandskrise i landdistrikterne i Amerika
- Hvilken celledel kontrollerer aktiviteterne?


