Hvordan er atomer relateret til molekyler i en prøve af forbindelse?
1. Byggesten:
* atomer: Individuelle, små partikler med en kerne (protoner og neutroner) og elektroner, der kredser om kernen. De repræsenterer den enkleste form af et element.
* molekyler: Form, når to eller flere atomer binder sig sammen gennem deling eller overførsel af elektroner. Disse obligationer skaber en stabil enhed.
2. Forbindelser vs. elementer:
* elementer: Består af kun en type atom (f.eks. Rent guld, iltgas).
* Forbindelser: Består af to eller flere forskellige typer atomer bundet sammen (f.eks. Vand (H₂O), kuldioxid (CO₂)).
3. Kemiske formler:
* Repræsenterer molekyler: Kemiske formler bruger symboler til hvert atom og underskrifter til at indikere antallet af hver type atom, der er til stede i et molekyle (f.eks. H₂O - to hydrogenatomer og et iltatom).
* Repræsenterer forbindelser: Kemiske formler repræsenterer sammensætningen af hele forbindelsen, der viser de typer og proportioner af de tilstedeværende atomer.
4. Eksempler:
* vand (H₂O): To hydrogenatomer binder sig med et iltatom til dannelse af et vandmolekyle. En prøve af vand indeholder mange vandmolekyler.
* natriumchlorid (NaCl): Et natriumatombindinger med et chloratom til dannelse af et natriumchloridmolekyle. En prøve af bordsalt indeholder mange natriumchloridmolekyler.
Kortfattet:
* Atomer er de grundlæggende byggesten, mens molekyler er grupper af atomer, der holdes sammen af kemiske bindinger.
* Forbindelser dannes af forskellige typer atomer bundet sammen, hvilket skaber molekyler med unikke egenskaber.
* Kemiske formler giver en kortfattet repræsentation af atomerne og deres forhold i et molekyle eller forbindelse.
Sidste artikelHvad er den kemiske ligning til reaktion af triethylamin med HCI?
Næste artikelHvad er en ionisk binding?
 Varme artikler
Varme artikler
-
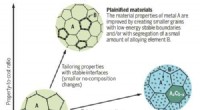 Plainification lover at forbedre materielle bæredygtighedMaterialernes ydeevne forbedres ofte ved at stabilisere grænseflader mellem korn ved at legere med andre elementer. (Billede af SYNL) Omfattende legering gør materialeudvikling mere afhængig af kn
Plainification lover at forbedre materielle bæredygtighedMaterialernes ydeevne forbedres ofte ved at stabilisere grænseflader mellem korn ved at legere med andre elementer. (Billede af SYNL) Omfattende legering gør materialeudvikling mere afhængig af kn -
 Kombination af mikrobielle og kemiske fingeraftryk til retsmedicinske applikationerUC San Diego-forskere udviklede et open source-værktøj kaldet ili til at kortlægge data om bakterier og molekyler på en 3D-model af et kontor. Kredit:University of California - San Diego Forskere
Kombination af mikrobielle og kemiske fingeraftryk til retsmedicinske applikationerUC San Diego-forskere udviklede et open source-værktøj kaldet ili til at kortlægge data om bakterier og molekyler på en 3D-model af et kontor. Kredit:University of California - San Diego Forskere -
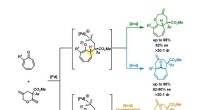 Divergent syntese af bicykliske mellemstore ringstrukturerFigur viser reaktionsvejene for den divergerende syntese af tre klasser af forbindelser. Ved at bruge det samme sæt af udgangsmaterialer og palladiumkatalysator, men udsat for forskellige reaktionsbet
Divergent syntese af bicykliske mellemstore ringstrukturerFigur viser reaktionsvejene for den divergerende syntese af tre klasser af forbindelser. Ved at bruge det samme sæt af udgangsmaterialer og palladiumkatalysator, men udsat for forskellige reaktionsbet -
 Motion er godt for din hud:Et protein efterligner nogle antialdringseffekter hos musForskere forstår endnu ikke virkningerne af aldring på de cellulære processer, der er involveret i hudheling. Justin Crane, en assisterende professor i biologi på Northeastern, og Wesley Wong, en fjer
Motion er godt for din hud:Et protein efterligner nogle antialdringseffekter hos musForskere forstår endnu ikke virkningerne af aldring på de cellulære processer, der er involveret i hudheling. Justin Crane, en assisterende professor i biologi på Northeastern, og Wesley Wong, en fjer
- Hvorfor er det vigtigt for planternes rod og skyde -system at arbejde sammen?
- Hvilken slags udbrud havde MT Etna?
- Hvis en 120V transformer har 200 omdrejninger den sekundære vikling 20, hvad er der spænding?
- Universitetsstuderende, fisk viser overraskende ligheder i numerisk tilnærmelse
- Anvendelse af havvand
- Blockbuster antitrust-retssag over AT&T, Time Warner-fusionen begynder


