Hvor mange valenselektroner har CO3 2-?
1. Valenselektroner af individuelle atomer:
* carbon (c): Gruppe 14, 4 valenselektroner
* ilt (O): Gruppe 16, 6 Valenselektroner
2. Samlede valenselektroner (ignorering af ladning):
* Carbon:1 atom * 4 elektroner =4 elektroner
* Ilt:3 atomer * 6 elektroner =18 elektroner
* I alt:4 + 18 =22 elektroner
3. Konto for gebyret:
* 2- ladningen indikerer, at ionen har fået to ekstra elektroner.
* Tilføj 2 til det samlede antal:22 + 2 =24 elektroner
Derfor har carbonationen (co₃²⁻) 24 valenselektroner.
 Varme artikler
Varme artikler
-
 Video:Mærkelige ideer til at bekæmpe klimaændringerKredit:The American Chemical Society Der er ting, du kan gøre lige nu for at hjælpe vores klima – som at investere i vedvarende energi. Men i dag om reaktioner, vi graver i et par af de mærkeligs
Video:Mærkelige ideer til at bekæmpe klimaændringerKredit:The American Chemical Society Der er ting, du kan gøre lige nu for at hjælpe vores klima – som at investere i vedvarende energi. Men i dag om reaktioner, vi graver i et par af de mærkeligs -
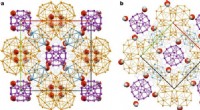 To Frank-Kasper faser i saltkrystalstrukturer observereten, Fase 1. b, Fase 2. Klynger A1, A2, B og C er farvet i lilla, orange, blå og grå, henholdsvis. I begge strukturer, lidelse er blevet fjernet for klarhedens skyld. Chlorider er blevet forbundet for
To Frank-Kasper faser i saltkrystalstrukturer observereten, Fase 1. b, Fase 2. Klynger A1, A2, B og C er farvet i lilla, orange, blå og grå, henholdsvis. I begge strukturer, lidelse er blevet fjernet for klarhedens skyld. Chlorider er blevet forbundet for -
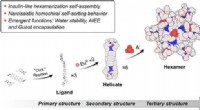 Hexameriske lanthanid-organiske kapsler med tertiær struktur, nye funktionerKredit: Journal of the American Chemical Society (2021). DOI:10.1021/jacs.1c01168 Metalrettede samlinger er blevet en meget brugt tilgang til at designe sofistikerede og multifunktionelle kunstig
Hexameriske lanthanid-organiske kapsler med tertiær struktur, nye funktionerKredit: Journal of the American Chemical Society (2021). DOI:10.1021/jacs.1c01168 Metalrettede samlinger er blevet en meget brugt tilgang til at designe sofistikerede og multifunktionelle kunstig -
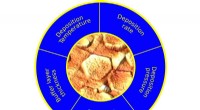 Statistiske design fremskynder optimeringen af lagdelte 2-D krystallerOptimering og vækst af tekstur Sb 2 Te 3 krystal ved statistisk design af eksperiment (DoE). Statistisk signifikante aflejringsfaktorer såsom temperatur, tryk, vækstrate, buffermaterialer, og buff
Statistiske design fremskynder optimeringen af lagdelte 2-D krystallerOptimering og vækst af tekstur Sb 2 Te 3 krystal ved statistisk design af eksperiment (DoE). Statistisk signifikante aflejringsfaktorer såsom temperatur, tryk, vækstrate, buffermaterialer, og buff


