Hvordan producerer hydrolysen af calciumcarbid tilfældigvis en acetylengas ved hjælp af varme?
reaktionen:
Calciumcarbid reagerer med vand (H₂O) for at producere acetylengas og calciumhydroxid (Ca (OH) ₂).
CAC₂ (S) + 2H₂O (L) → C₂H₂ (G) + CA (OH) ₂ (AQ)
Forklaring:
* Calciumcarbid (CAC₂) er en meget reaktiv forbindelse. Det indeholder carbonatomer bundet til hinanden med en tredobbelt binding.
* vand (H₂O) fungerer som reaktant. Hydrogenatomerne i vand tiltrækkes af carbonatomerne i calciumcarbid.
* Reaktionen fortsætter ved brud på den tredobbelte binding i calciumcarbid. Dette frigiver energi, hvilket gør reaktionen eksoterm.
* acetylengas (C₂H₂) dannes Carbonatomerne fra calciumcarbid kombineres med hydrogenatomer fra vand for at danne acetylenmolekylet.
* Calciumhydroxid (CA (OH) ₂) dannes også. Dette er et biprodukt af reaktionen, og det opløses i vand.
Heat's rolle:
Mens reaktionen i sig selv frigiver varme, er anvendelse af varme ikke nødvendig for at starte reaktionen . Faktisk er reaktionen ret kraftig og kan endda være eksplosiv, hvis reaktionshastigheden er for hurtig.
Praktisk anvendelse:
* Denne reaktion bruges industrielt til at producere acetylengas.
* Acetylen er en brandfarlig gas, der bruges til svejsning og skæring af metaller på grund af dets høje varmeudgang.
sikkerhed:
* Calciumcarbid er et farligt materiale, da det reagerer voldsomt med vand.
* Reaktionen skal altid udføres i et godt ventileret område og med passende sikkerhedsforanstaltninger.
Sidste artikelHvor mange mol kobber er til stede i 75,92 g?
Næste artikelHvor mange valenselektroner har CO3 2-?
 Varme artikler
Varme artikler
-
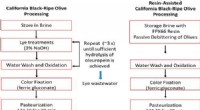 En grønnere måde at tage bitterheden ud af olivenKredit:American Chemical Society Oliven er en del af middelhavskosten, som har været forbundet med en reduceret forekomst af hjerte-kar-sygdomme, Alzheimers sygdom og andre tilstande. Imidlertid,
En grønnere måde at tage bitterheden ud af olivenKredit:American Chemical Society Oliven er en del af middelhavskosten, som har været forbundet med en reduceret forekomst af hjerte-kar-sygdomme, Alzheimers sygdom og andre tilstande. Imidlertid, -
 Retsmedicinere låser op for unikke kemiske signaturer i dækTeamet fra University of Central Florida brugte laserinduceret nedbrydningsspektroskopi (LIBS) på hver prøve. Teknikken fokuserer en laser på dækprøven, som skaber et mikroskopisk plasma, der udsender
Retsmedicinere låser op for unikke kemiske signaturer i dækTeamet fra University of Central Florida brugte laserinduceret nedbrydningsspektroskopi (LIBS) på hver prøve. Teknikken fokuserer en laser på dækprøven, som skaber et mikroskopisk plasma, der udsender -
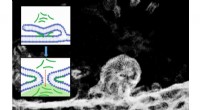 Hvordan trænger peptider ind i celler? To sider af samme møntElektronmikroskopibillede af en todelt cellemembran og det tilsvarende molekylære skema for processen. Kredit:@ IOCB Prag Den simple transport af lægemidler direkte ind i cellerne er et af de prim
Hvordan trænger peptider ind i celler? To sider af samme møntElektronmikroskopibillede af en todelt cellemembran og det tilsvarende molekylære skema for processen. Kredit:@ IOCB Prag Den simple transport af lægemidler direkte ind i cellerne er et af de prim -
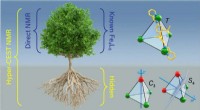 Hyper-CEST NMR-teknik afslører manglende struktur af et nyt beholdermolekyleHyper-CEST som ultrafølsomt NMR-spektroskopiværktøj afslører to tidligere skjulte strukturer af metalorganiske bure. Kredit:Barth van Rossum, FMP Ved hjælp af Hyper-CEST NMR-teknikken har holdet le
Hyper-CEST NMR-teknik afslører manglende struktur af et nyt beholdermolekyleHyper-CEST som ultrafølsomt NMR-spektroskopiværktøj afslører to tidligere skjulte strukturer af metalorganiske bure. Kredit:Barth van Rossum, FMP Ved hjælp af Hyper-CEST NMR-teknikken har holdet le
- Vil NASAs TESS-rumfartøj revolutionere eksoplanetjagten?
- Hvordan brugte Wegener fossile beviser til at støtte sin hypotese?
- Arsen i husholdningsbrøndvand kan påvirke to millioner mennesker i USA
- Hvad er det bedste brændstof til at drive en ø?
- I hvilken grad fryser saltvand i is?
- Hvad er det modsatte af en ionbinding?


