Hvilken er mere polær NH3 eller H2O?
Her er hvorfor:
* Elektronegativitet: Oxygen (O) er mere elektronegativ end nitrogen (N), hvilket betyder, at det tiltrækker elektroner stærkere. Dette skaber en større forskel i elektronegativitet mellem det centrale atom og hydrogenatomerne i vand sammenlignet med ammoniak.
* molekylær geometri: Vand har en bøjet molekylær geometri på grund af de to ensomme par elektroner på iltatomet, mens ammoniak har en trigonal pyramidal geometri. Denne bøjede form i vand forbedrer polariteten ved at koncentrere den negative ladning mod iltatomet.
* dipolmoment: Den større forskel i elektronegativitet og den bøjede geometri af vand fører til et højere dipolmoment (et mål for polaritet) sammenlignet med ammoniak.
Kortfattet:
* Vand har en større forskel i elektronegativitet mellem ilt og brint.
* Water's bøjede geometri forbedrer sin polaritet yderligere.
* Som et resultat har vand et højere dipolmoment og er mere polær end ammoniak.
Sidste artikelHvordan skriver du ilt?
Næste artikelHvilken slags klima er bedst egnet til kemisk forvitring?
 Varme artikler
Varme artikler
-
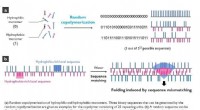 Ny polymer mesofasestruktur opdagetKredit:Korea Advanced Institute of Science and Technology Polymerer, store molekyler, der består af gentagne mindre molekyler kaldet monomerer, findes i næsten alt, hvad vi bruger i vores daglige l
Ny polymer mesofasestruktur opdagetKredit:Korea Advanced Institute of Science and Technology Polymerer, store molekyler, der består af gentagne mindre molekyler kaldet monomerer, findes i næsten alt, hvad vi bruger i vores daglige l -
 Ostfremstilling afhænger af mælkeproteiner for at danne strukturKredit:Pixabay/CC0 Public Domain Osteproduktion er afhængig af koagulation af mælkeproteiner til en gelmatrix efter tilsætning af osteløbe. Mælk, der ikke koagulerer (NC) under optimale forhold på
Ostfremstilling afhænger af mælkeproteiner for at danne strukturKredit:Pixabay/CC0 Public Domain Osteproduktion er afhængig af koagulation af mælkeproteiner til en gelmatrix efter tilsætning af osteløbe. Mælk, der ikke koagulerer (NC) under optimale forhold på -
 Forskere rapporterer om ny klasse af polyethylenkatalysatorerOlafs Daugulis, Robert A. Welch Chair of Chemistry ved University of Houston, ledet et team, der opdagede en ny klasse af katalysatorer til fremstilling af ultra-højvægts polyethylen. Kredit:Universit
Forskere rapporterer om ny klasse af polyethylenkatalysatorerOlafs Daugulis, Robert A. Welch Chair of Chemistry ved University of Houston, ledet et team, der opdagede en ny klasse af katalysatorer til fremstilling af ultra-højvægts polyethylen. Kredit:Universit -
 Klarhed nødvendig i klassificeringssystemer til forarbejdede fødevarerKredit:Pixabay/CC0 Public Domain Nuværende fødevareklassifikationssystemer for forarbejdede fødevarer mangler konsistens og konsensus, der ofte fører til forvirring og debat, selv blandt forskere,
Klarhed nødvendig i klassificeringssystemer til forarbejdede fødevarerKredit:Pixabay/CC0 Public Domain Nuværende fødevareklassifikationssystemer for forarbejdede fødevarer mangler konsistens og konsensus, der ofte fører til forvirring og debat, selv blandt forskere,
- Forskelle i wolframisotoper viser, at jordens overflade er dannet ujævnt
- Hvordan beregnes størrelsen af jordskælv?
- Organiseret kaos i enzymkomplekset – overraskende indsigt og nye perspektiver
- Nanopartikler giver forstærkning til usynlige beslag inden for ortodonti
- Undersøgelse udforsker, hvordan læsere på partiske nyhedssider reagerer på udfordrende nyhedsbeg…
- San Francisco forbyder brug af ansigtsgenkendelse af politi og regering


