Hvordan fremstilles chloridioner?
Her er en sammenbrud:
* kloratom: Et kloratom har 17 elektroner. Dens elektroniske konfiguration er 2, 8, 7. Dette betyder, at den har 7 elektroner i sin yderste skal, hvilket gør den meget reaktiv.
* ionisering: Når et chloratom får et elektron, bliver det en chloridion. Denne elektron fylder den yderste skal, hvilket giver den en stabil elektronisk konfiguration af 2, 8, 8.
Processen kan repræsenteres af følgende ligning:
cl + e- → cl-
hvor:
* Cl repræsenterer et kloratom
* e-repræsenterer en elektron
* Cl- repræsenterer en chloridion
almindelige måder chloridioner dannes:
* ionisk binding: Når klor reagerer med et metal, får det et elektron fra metalatomet og danner en chloridion. Dette resulterer i en ionisk binding, hvor metalkationen og chloridanionen tiltrækker hinanden.
* opløste salte: Mange salte, såsom natriumchlorid (NaCI), indeholder chloridioner. Når disse salte opløses i vand, adskiller chloridionerne sig fra saltet og bliver fri i opløsning.
Chloridioner er vigtige for mange biologiske processer, herunder opretholdelse af væskebalance, nervegenressultat og syre-base-balance.
Sidste artikelHvad er formlen for carbon pentachlorid?
Næste artikelHvor mange mol brint kræves for at producere 18,00 ammoniak?
 Varme artikler
Varme artikler
-
 Sensoren kan registrere fordærvet mælk, før den åbnesDen eksperimentelle opsætning til påvisning af de flygtige forbindelser i mælk, med de lyserøde nanopartikler set over væsken. Kredit:WSU Udløbsdatoer på mælk kan i sidste ende blive fortid med ny
Sensoren kan registrere fordærvet mælk, før den åbnesDen eksperimentelle opsætning til påvisning af de flygtige forbindelser i mælk, med de lyserøde nanopartikler set over væsken. Kredit:WSU Udløbsdatoer på mælk kan i sidste ende blive fortid med ny -
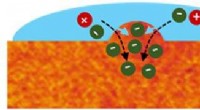 For at forbinde biologi med elektronik, være stiv, alligevel fleksibelEt skematisk billede af P3HT-filmen, viser områder, der er i stand til subtilt at svulme op for at lukke ionmolekyler ind. Kredit:Rajiv Giridharagopal Problemet er en grundlæggende uforenelighed i
For at forbinde biologi med elektronik, være stiv, alligevel fleksibelEt skematisk billede af P3HT-filmen, viser områder, der er i stand til subtilt at svulme op for at lukke ionmolekyler ind. Kredit:Rajiv Giridharagopal Problemet er en grundlæggende uforenelighed i -
 Enhed forvandler skaller af havdyr til kraft til medicinsk, augmented reality, mobiltelefonenhederEt Purdue-team er ved at omdanne rejeskalmateriale til en funktionel enhed til at generere elektricitet. Kredit:Purdue University En innovation, der bruger materiale, der stammer fra skaller fra k
Enhed forvandler skaller af havdyr til kraft til medicinsk, augmented reality, mobiltelefonenhederEt Purdue-team er ved at omdanne rejeskalmateriale til en funktionel enhed til at generere elektricitet. Kredit:Purdue University En innovation, der bruger materiale, der stammer fra skaller fra k -
 Ny rekord i blyfri halogenid-dobbeltperovskitterLuminescens -ejendommen for Cs 2 AgBi 1-x I x Cl 6 (0
Ny rekord i blyfri halogenid-dobbeltperovskitterLuminescens -ejendommen for Cs 2 AgBi 1-x I x Cl 6 (0- Hvad er nogle eksempler på multicellulære mikroorganismer og sangecellede mikroorganismer?
- Sådan konverteres tanganter til grader
- Ser nattehimlen ens ud overalt?
- Brug af kulstof nanorør i lithium-batterier kan dramatisk forbedre energikapaciteten
- Astronomer udpeger det bedste sted på Jorden for et teleskop:Højt på et koldt antarktisk plateau
- Sætter den kinetiske molekylære teori, at alle partikler af stof altid er i bevægelse?


