Hvor mange Na -ioner er der i 4,2 g NaCl?
1. Beregn den molære masse af NaCl:
* NA:22,99 g/mol
* Cl:35,45 g/mol
* NaCl:22,99 + 35,45 =58,44 g/mol
2. Beregn molen af NaCl:
* mol =masse / molær masse
* mol =4,2 g / 58,44 g / mol =0,0718 mol
3. Da der er et na ion pr. NaCl -molekyle, er der 0,0718 mol Na -ioner.
4. Beregn antallet af NA -ioner:
* Antal ioner =mol * Avogadros nummer
* Antal ioner =0,0718 mol * 6,022 x 10^23 ioner/mol
* Antal NA -ioner =4,32 x 10^22 ioner
Derfor er der ca. 4,32 x 10^22 na -ioner i 4,2 g NaCl.
Sidste artikelHvordan har arbejdet fra kemikere påvirket miljøet?
Næste artikelHvad er PH af kobberchlorid?
 Varme artikler
Varme artikler
-
 Forskere rapporterer om effektiv platformsteknologi til fremstilling af cephalosporin-antibiotikaKredit:CC0 Public Domain Antibiotika redder utallige menneskeliv - moderne medicin uden dem er utænkelig. Den største volumenandel af industrielt fremstillede antibiotika i dag er cephalosporiner,
Forskere rapporterer om effektiv platformsteknologi til fremstilling af cephalosporin-antibiotikaKredit:CC0 Public Domain Antibiotika redder utallige menneskeliv - moderne medicin uden dem er utænkelig. Den største volumenandel af industrielt fremstillede antibiotika i dag er cephalosporiner, -
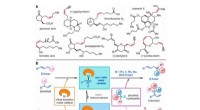 Iridium-katalyserede Z-tilbageholdende asymmetriske allyliske substitutionsreaktionerStrategi for konstruktion af Z-olefiner via asymmetriske allyliske substitutionsreaktioner katalyseret af overgangsmetalkatalysatorer. (A) Udvalgte naturlige produkter indeholdende Z-olefiner med homo
Iridium-katalyserede Z-tilbageholdende asymmetriske allyliske substitutionsreaktionerStrategi for konstruktion af Z-olefiner via asymmetriske allyliske substitutionsreaktioner katalyseret af overgangsmetalkatalysatorer. (A) Udvalgte naturlige produkter indeholdende Z-olefiner med homo -
 pH-værdien af calciumioner kontrollerer ionkanalåbningenEn dørvogterring:Det ekstracytosoliske/lumenale domæne af den menneskelige TRPML2-ionkanal, hvis struktur denne undersøgelse belyste for første gang, fungerer som en pH-afhængig calciumregulator. Det
pH-værdien af calciumioner kontrollerer ionkanalåbningenEn dørvogterring:Det ekstracytosoliske/lumenale domæne af den menneskelige TRPML2-ionkanal, hvis struktur denne undersøgelse belyste for første gang, fungerer som en pH-afhængig calciumregulator. Det -
 Kemikalieproducenter er imod nye tarifferKredit:CC0 Public Domain I juni, kemiske producenter konvergerede om Washington, D.C., at opfordre US Trade Representative Office (USTR) til at fjerne visse kemikalier fra en ny liste over toldsat
Kemikalieproducenter er imod nye tarifferKredit:CC0 Public Domain I juni, kemiske producenter konvergerede om Washington, D.C., at opfordre US Trade Representative Office (USTR) til at fjerne visse kemikalier fra en ny liste over toldsat


