Hvorfor er carbontetrachlorid og vand ikke blanding?
* Polaritet: Vand er et polært molekyle. Dette betyder, at det har en lidt positiv ende (hydrogenatomer) og en lidt negativ ende (iltatom) på grund af ujævn deling af elektroner. Carbon-tetrachlorid er på den anden side et ikke-polært molekyle. Dens symmetriske struktur og elektronegativiteten af kloratomer fører til en jævn fordeling af elektroner.
* "som opløser som": En generel regel inden for kemi er, at "som opløser som." Polære opløsningsmidler opløser polære opløste stoffer, og ikke-polære opløsningsmidler opløser ikke-polære opløste stoffer. Vand, der er et polært opløsningsmiddel, kan effektivt interagere med andre polære molekyler gennem brintbinding. Carbon-tetrachlorid, der er ikke-polær, kan ikke danne så stærke interaktioner med vand.
* Intermolekylære kræfter: Vandmolekyler danner stærke brintbindinger med hinanden og skaber et sammenhængende netværk. Carbon-tetrachlorid har med dets ikke-polære karakter svagere intermolekylære kræfter (London-spredningskræfter). Denne forskel i intermolekylære kræfter forhindrer de to stoffer i at blande og danne en homogen opløsning.
Kortfattet: Uanskeligheden af carbontetrachlorid og vand stammer fra den grundlæggende forskel i deres polariteter og den resulterende manglende evne til deres molekyler til at interagere positivt. De adskiller sig i forskellige lag, når de blandes på grund af deres kontrasterende molekylære interaktioner.
Sidste artikel2 i H2O er et eksempel på?
Næste artikelHvad sker der, når et fluoratom bliver melidion i kemisk reaktion?
 Varme artikler
Varme artikler
-
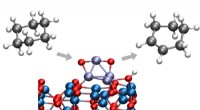 Forskere er banebrydende for den nye kemiske konverteringsproces ved lav temperaturArgonne -kemikere har identificeret en måde at konvertere cyclohexan til cyclohexen eller cyclohexadien, begge vigtige kemikalier i en lang række industrielle processer. Den nye proces finder sted ved
Forskere er banebrydende for den nye kemiske konverteringsproces ved lav temperaturArgonne -kemikere har identificeret en måde at konvertere cyclohexan til cyclohexen eller cyclohexadien, begge vigtige kemikalier i en lang række industrielle processer. Den nye proces finder sted ved -
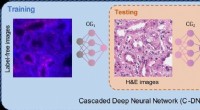 Kemikaliefri genfarvning af væv ved hjælp af dyb læringVirtuel genfarvning af væv ved hjælp af kaskadede dybe neurale netværk. Kredit:Ozcan Lab @ UCLA. Vævsbaseret diagnosticering af sygdomme er afhængig af den visuelle inspektion af biopsierede vævspr
Kemikaliefri genfarvning af væv ved hjælp af dyb læringVirtuel genfarvning af væv ved hjælp af kaskadede dybe neurale netværk. Kredit:Ozcan Lab @ UCLA. Vævsbaseret diagnosticering af sygdomme er afhængig af den visuelle inspektion af biopsierede vævspr -
 Skoler med molekylær fisk kunne forbedre skærmeSkoler af solitons form til klynger. Kredit:Smalyukh lab Tag et dyk ned i det, der kan være verdens mindste koralrev. Forskere ved University of Colorado Boulder bruger en type materiale kaldet fl
Skoler med molekylær fisk kunne forbedre skærmeSkoler af solitons form til klynger. Kredit:Smalyukh lab Tag et dyk ned i det, der kan være verdens mindste koralrev. Forskere ved University of Colorado Boulder bruger en type materiale kaldet fl -
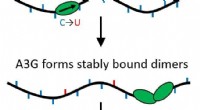 En hvis ved at redigere, to ved vejspærring:Humant protein bekæmper HIV som monomer og dimerForskning for nylig offentliggjort i Naturkommunikation undersøger mulighederne for et humant protein, der hæmmer HIV-1, APOBEC3G (A3G). Papiret fremhæver arbejdet af Northeastern Physics professor
En hvis ved at redigere, to ved vejspærring:Humant protein bekæmper HIV som monomer og dimerForskning for nylig offentliggjort i Naturkommunikation undersøger mulighederne for et humant protein, der hæmmer HIV-1, APOBEC3G (A3G). Papiret fremhæver arbejdet af Northeastern Physics professor
- Hvordan laver man en hjemmelavet hoppekugle lavet af et æg
- COVID ændrede aflevering og afhentning. Men forældre kan stadig have et stærkt forhold til deres …
- Hvad er massen af et atom koncentreret om?
- Hvilken bjergkæde dannede sig, da pladen indeholdende indisk subkontinent bombede til kontinentet i…
- Har solen sin rotation og revolution?
- Hvorfor er Jorden grøn og blå?


