Hvor mange mol natriumhydroxid reagerer med 17 svovlsyre?
1. Afbalanceret kemisk ligning:
Den afbalancerede kemiske ligning for denne reaktion er:
2NAOH + H₂SO₄ → NA₂SO₄ + 2H₂O
Dette fortæller os, at 2 mol NaOH reagerer med 1 mol H₂so₄.
2. Vi er nødt til at kende koncentrationen af svovlsyren Du leverede "17 svovlsyre", men det er ikke en standardenhed. Mener du:
* 17 gram svovlsyre?
* 17 ml svovlsyre? (Vi har brug for koncentrationen, f.eks. 17 ml af 1 m svovlsyre)
* 17 mol svovlsyre?
Lad os antage, at du mente 17 gram svovlsyre.
3. Konverter gram af H₂so₄ til mol:
* Find den molære masse af H₂so₄:(2 x 1,01 g/mol) + (32,07 g/mol) + (4 x 16,00 g/mol) =98,08 g/mol
* Opdel massen af H₂so₄ ved dens molære masse:17 g / 98,08 g / mol =0,173 mol H₂so₄
4. Beregn mol af NaOH:
* Brug molforholdet fra den afbalancerede ligning:2 mol NaOH:1 mol H₂so₄
* Multiplicer molen af H₂so₄ med molforholdet:0,173 mol H₂so₄ * (2 mol NaOH / 1 mol H₂so₄) =0,346 mol NaOH
Derfor reagerer ca. 0,346 mol natriumhydroxid med 17 gram svovlsyre.
Vigtig note: Kontroller altid enhederne og sørg for, at du har de rigtige oplysninger, før du foretager beregninger.
Sidste artikelHvor mange elektroner er der i den ydre kobberskal?
Næste artikelHvad producerer natrium- og vandreaktion?
 Varme artikler
Varme artikler
-
 Nyt materiale tilbyder en miljøvenlig løsning til at omdanne spildvarme til energiKredit:Unsplash/CC0 Public Domain vedholdenhed, NASAs 2020 Mars rover, er drevet af noget meget ønskværdigt her på Jorden:en termoelektrisk enhed, som omdanner varme til nyttig elektricitet. På M
Nyt materiale tilbyder en miljøvenlig løsning til at omdanne spildvarme til energiKredit:Unsplash/CC0 Public Domain vedholdenhed, NASAs 2020 Mars rover, er drevet af noget meget ønskværdigt her på Jorden:en termoelektrisk enhed, som omdanner varme til nyttig elektricitet. På M -
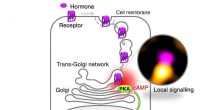 Hvordan receptorer for medicin virker inde i cellerNyopdaget mekanisme for GPCR-signalering ved trans-Golgi-netværket (TGN). Ved binding af et hormon (TSH), receptoren optages af cellen (internalisering) og transporteres til TGN, hvor det inducerer lo
Hvordan receptorer for medicin virker inde i cellerNyopdaget mekanisme for GPCR-signalering ved trans-Golgi-netværket (TGN). Ved binding af et hormon (TSH), receptoren optages af cellen (internalisering) og transporteres til TGN, hvor det inducerer lo -
 Forskere designer organisk katode til højtydende batterierHovedforfatter Zulipiya Shadike (til højre) er afbilledet ved NSLS-IIs XPD-strålelinje sammen med videnskabsmand og medforfatter Sanjit Ghose (til venstre). Kredit:Brookhaven National Laboratory F
Forskere designer organisk katode til højtydende batterierHovedforfatter Zulipiya Shadike (til højre) er afbilledet ved NSLS-IIs XPD-strålelinje sammen med videnskabsmand og medforfatter Sanjit Ghose (til venstre). Kredit:Brookhaven National Laboratory F -
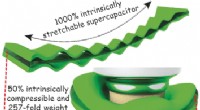 Super strækbar, superkomprimerbare superkondensatorerFleksibel, bærbar elektronik kræver lige så fleksibel, bærbare strømkilder. I journalen Angewandte Chemie , Kinesiske videnskabsmænd har introduceret en ekstraordinært strækbar og komprimerbar polye
Super strækbar, superkomprimerbare superkondensatorerFleksibel, bærbar elektronik kræver lige så fleksibel, bærbare strømkilder. I journalen Angewandte Chemie , Kinesiske videnskabsmænd har introduceret en ekstraordinært strækbar og komprimerbar polye


