Hvad er formelmassen på Na2CO3.10H2O?
1. Identificer elementerne og deres atommasser:
* na (natrium): 22,99 g/mol
* c (carbon): 12,01 g/mol
* o (ilt): 16,00 g/mol
* h (brint): 1,01 g/mol
2. Multiplicer atommassen for hvert element med dets underskrift i formlen:
* NA: 2 * 22,99 g/mol =45,98 g/mol
* C: 1 * 12,01 g/mol =12,01 g/mol
* o: 3 * 16,00 g/mol =48,00 g/mol
* h: 20 * 1,01 g/mol =20,20 g/mol
* o (fra vand): 10 * 16,00 g/mol =160,00 g/mol
3. Tilføj masserne af alle elementerne:
45,98 g/mol + 12,01 g/mol + 48,00 g/mol + 20,20 g/mol + 160,00 g/mol = 286,19 g/mol
Derfor er formelmassen af Na₂co₃ · 10H₂O 286,19 g/mol.
Sidste artikelHvis et kloratom vinder eller mister valenselektron, bliver det ladet partikel kaldet?
Næste artikelHvad er kilden til klor?
 Varme artikler
Varme artikler
-
 Ny model giver vingårde bedre data fra eksisterende testsKredit:CC0 Public Domain Når det kommer til vin, kemien skal være den rigtige for at få den bedste smag og fornemmelse. For at hjælpe vinproducenter med den kemi, et team af forskere ved Washingt
Ny model giver vingårde bedre data fra eksisterende testsKredit:CC0 Public Domain Når det kommer til vin, kemien skal være den rigtige for at få den bedste smag og fornemmelse. For at hjælpe vinproducenter med den kemi, et team af forskere ved Washingt -
 Hvad er det kemiske middel, der angiveligt blev brugt til at forgifte den russiske politiker Alexei …Cholinesterasehæmmere er ikke alle kemiske våben - de kan omfatte daglige pesticider. Kredit:Shutterstock Den medicinske evakuering af Alexei Navalnyj, den åbenhjertige politiske kritiker af Vladi
Hvad er det kemiske middel, der angiveligt blev brugt til at forgifte den russiske politiker Alexei …Cholinesterasehæmmere er ikke alle kemiske våben - de kan omfatte daglige pesticider. Kredit:Shutterstock Den medicinske evakuering af Alexei Navalnyj, den åbenhjertige politiske kritiker af Vladi -
 Bakterier kaprer konkurrentens latente fagSom viruspartikler, fager inficerer bakterier for at sikre deres egen fremgang. Kredit:Thomas Böttcher Denne målrettede kontrol med fager giver helt nye bioteknologiske og terapeutiske tilgange, f
Bakterier kaprer konkurrentens latente fagSom viruspartikler, fager inficerer bakterier for at sikre deres egen fremgang. Kredit:Thomas Böttcher Denne målrettede kontrol med fager giver helt nye bioteknologiske og terapeutiske tilgange, f -
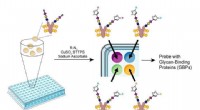 Ny TSRI-metode fremskynder undersøgelser af kulhydratbiologiEn ny metode til at samle et glycan-array. Kredit:Wu Lab / Scripps Research Institute 28. februar, 2018 - Næsten alle levende celler er besat med forgrenede kulhydratkæder kaldet glykaner. Glykane
Ny TSRI-metode fremskynder undersøgelser af kulhydratbiologiEn ny metode til at samle et glycan-array. Kredit:Wu Lab / Scripps Research Institute 28. februar, 2018 - Næsten alle levende celler er besat med forgrenede kulhydratkæder kaldet glykaner. Glykane
- Hvilket lag af atmosfæren ligger solen?
- Studie af akustiske grafenplasmoner baner vej for optoelektroniske applikationer
- Gå forbi shiraz, tak:hvordan Australiens vinindustri kan tilpasse sig klimaændringer
- Fugleneuroner bruger tre gange mindre glukose end pattedyrneuroner
- Hvordan bruges videnskabelige data som bevis for at udvikle teorier beskriver universets oprindelse?…
- Hvilken slags klippe dannes af vind og blæser sand?


