Hvilket stof oxideres, når natrium reagerer med klorgas?
* Oxidation er tabet af elektroner.
* reduktion er gevinsten af elektroner.
I reaktionen:
2NA (S) + Cl₂ (G) → 2NACl (S)
* Natrium (NA) starter som et neutralt atom med en valenselektron.
* Chlor (CL) starter som et diatomisk molekyle med syv valenselektroner pr. Atom.
* Natrium mister sin valenselektron for at blive en positivt ladet ion (Na+).
* Klor får et elektron for at blive en negativt ladet ion (Cl-).
Da natrium mister En elektron, det gennemgår oxidation . Chlor Gains En elektron, så det gennemgår reduktion .
Sidste artikelEr fisk en fast væske eller en gas?
Næste artikelHvad er den kemiske formel for Tin IV -oxid?
 Varme artikler
Varme artikler
-
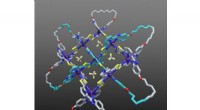 Forskere opdager en ny type molekylær knude ved hjælp af røntgendiffraktionsteknikkerDavid Leigh, University of Manchester. Forskere har udviklet en måde at flette tre molekylære tråde, så det er muligt at lave strammere og mere komplekse knuder, end det tidligere har været muligt
Forskere opdager en ny type molekylær knude ved hjælp af røntgendiffraktionsteknikkerDavid Leigh, University of Manchester. Forskere har udviklet en måde at flette tre molekylære tråde, så det er muligt at lave strammere og mere komplekse knuder, end det tidligere har været muligt -
 Materialeinformatik afslører ny klasse af superhårde legeringerEt røntgenenergi-dispersiv spektroskopi (EDS) kort over den støbte mikrostruktur af en hård legering forudsagt fra Lehigh University forskeres analyse. Bogstaver er røntgenintensitetskort forbundet me
Materialeinformatik afslører ny klasse af superhårde legeringerEt røntgenenergi-dispersiv spektroskopi (EDS) kort over den støbte mikrostruktur af en hård legering forudsagt fra Lehigh University forskeres analyse. Bogstaver er røntgenintensitetskort forbundet me -
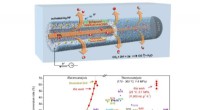 Ny sølv hulfiber booster CO2-elektroreduktionSkematisk illustration af hulfiberelektrode til at øge CO2-reduktionen til CO. Kredit:SARI Et forskerhold ledet af Profs. Wei Wei og Chen Wei fra Shanghai Advanced Research Institute (SARI) fra det
Ny sølv hulfiber booster CO2-elektroreduktionSkematisk illustration af hulfiberelektrode til at øge CO2-reduktionen til CO. Kredit:SARI Et forskerhold ledet af Profs. Wei Wei og Chen Wei fra Shanghai Advanced Research Institute (SARI) fra det -
 Opdagelse af nye lægemidler er en lang og dyr proces:Kemiske forbindelser, som duper screeningsvær…Kredit:Pixabay/CC0 Public Domain Moderne lægemiddelopdagelse er en dyr og kompliceret proces. Hundredvis af videnskabsmænd og mindst et årti er ofte påkrævet for at producere en enkelt medicin. Et
Opdagelse af nye lægemidler er en lang og dyr proces:Kemiske forbindelser, som duper screeningsvær…Kredit:Pixabay/CC0 Public Domain Moderne lægemiddelopdagelse er en dyr og kompliceret proces. Hundredvis af videnskabsmænd og mindst et årti er ofte påkrævet for at producere en enkelt medicin. Et
- Gruppen arbejder på at udvikle topologisk superleder
- Californiens vandmyndigheder ved ikke, hvor meget deres rør lækker, viser rapporten
- Hvad er én ting et molekyles form kan påvirke?
- Hvordan relaterer kraft og bevægelse?
- Hvilken sæson kan konstellationerne ses?
- Cruise opdaterer software til autonome køretøjer efter styrt


