Hvorfor ses ikke aflejringer af rent natriummetal eller kalium i naturen?
* Høj reaktivitet: Natrium og kalium er meget reaktive alkalimetaller. De reagerer let med luft (ilt) for at danne oxider og med vand til dannelse af hydroxider og frigiver brintgas. Denne reaktivitet gør dem meget ustabile i deres elementære form.
* Elektropositiv karakter: Både natrium og kalium er meget elektropositive, hvilket betyder, at de let mister elektroner for at blive positivt ladede ioner. Dette gør dem tilbøjelige til at reagere med andre elementer og danne forbindelser i stedet for at eksistere i deres rene metalliske tilstand.
* forekomst i forbindelser: Disse elementer er rigelige i naturen, men findes næsten altid i sammensat form.
* natrium: Almindeligvis findes som natriumchlorid (bordsalt), natriumnitrat (findes i Chile) og forskellige andre mineraler.
* kalium: Fundet i mineraler som kaliumchlorid (sylvite), kaliumnitrat (NITER) og feltspat.
Kortfattet: Den ekstreme reaktivitet af natrium og kalium gør det umuligt for dem at eksistere som rene metaller i det naturlige miljø. De findes altid i kombination med andre elementer og danner forskellige forbindelser.
Sidste artikelNår natrium og klorbinding, hvilken slags er dette?
Næste artikelEr KCl en blanding eller rent stof?
 Varme artikler
Varme artikler
-
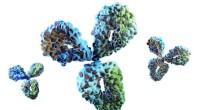 I et felt, hvor mindre er bedre, forskere opdager verdens mindste antistofferFuldstændig struktur af et antistof, viser dens domæner. Kredit:University of Bath Forskere ved University of Bath i Storbritannien og biofarmavirksomheden UCB har fundet en måde at producere mini
I et felt, hvor mindre er bedre, forskere opdager verdens mindste antistofferFuldstændig struktur af et antistof, viser dens domæner. Kredit:University of Bath Forskere ved University of Bath i Storbritannien og biofarmavirksomheden UCB har fundet en måde at producere mini -
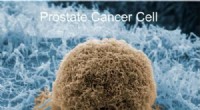 Billig detektor er som velcro til kræftcellerKredit:American Chemical Society Forskere har udviklet en ny type sensor, der fungerer som velcro for prostatacancerceller, klæbe dem på et modificeret matglas, som dem, der bruges i naturfag, så
Billig detektor er som velcro til kræftcellerKredit:American Chemical Society Forskere har udviklet en ny type sensor, der fungerer som velcro for prostatacancerceller, klæbe dem på et modificeret matglas, som dem, der bruges i naturfag, så -
 Udførelse af kemi i flydende dråberKredit:California Institute of Technology Kunne kemikere være klar til at droppe det ærværdige reagensglas, selve symbolet på kemi i mange menneskers sind? Måske ikke helt endnu men Caltechs Jack
Udførelse af kemi i flydende dråberKredit:California Institute of Technology Kunne kemikere være klar til at droppe det ærværdige reagensglas, selve symbolet på kemi i mange menneskers sind? Måske ikke helt endnu men Caltechs Jack -
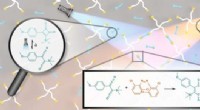 Skærende lysstråler er nøglen til transformativt 3D-printerpotentialeSkematisk reaktionsoversigt. Tofarvet aktivering af et stabilt cyclobutenedion (UV-lys) og rødforskudt ortho-substitueret tetrachlorid-azobenzen (orange lys) muliggør dannelse af ligeret produkt ved p
Skærende lysstråler er nøglen til transformativt 3D-printerpotentialeSkematisk reaktionsoversigt. Tofarvet aktivering af et stabilt cyclobutenedion (UV-lys) og rødforskudt ortho-substitueret tetrachlorid-azobenzen (orange lys) muliggør dannelse af ligeret produkt ved p
- Hvad er saltvandingredienser?
- Nuclear Energy Vs. Fossilt brændstof
- Hvem er den videnskabsmand, der hævder, at der findes liv på Mars?
- Hvert år i Australien, naturen dyrker 8 nye træer til dig – men det alene løser ikke klimaændrin…
- Ny undersøgelse undersøger, hvordan miljøfaktorer påvirker brugen af svingporte
- Bedre batterier fra bunden og op


