Hvad er molekylstrukturen for Na2PO3F?
* ionisk natur: Na2PO3F er en ionisk forbindelse, hvilket betyder, at den dannes ved elektrostatisk tiltrækning mellem positivt ladede natriumioner (Na+) og negativt ladede fluorophosphationer (PO3F2-).
* Ingen diskrete molekyler: Der er ingen tydelige, kovalent bundet PO3F2- molekyler i fast tilstand. I stedet er fluorophosphationerne sammenkoblet i et mere komplekst 3D -netværk.
Så hvordan repræsenterer det?
* Formelenhed: Den kemiske formel Na2PO3F repræsenterer det enkleste forhold mellem ioner i forbindelsen.
* strukturelt diagram over fluorophosphationen (PO3F2-): Du kan tegne en Lewis -struktur, der viser forbindelsen og arrangementet af atomer inden for fluorofosfationen:
- Det centrale fosforatom er omgivet af tre iltatomer og et fluoratom.
- To af iltatomerne er hver forbundet til en enkelt binding med fosfor og har en formel negativ ladning.
- Det tredje ilt er dobbeltbundet til fosfor.
- Fluoratomet er enkeltbundet til fosfor.
Vigtig note: Det faktiske arrangement af disse ioner i fast tilstand er kompleks og involverer sandsynligvis et netværk af sammenkoblede fluorophosphationer. Denne netværksstruktur er svær at repræsentere i et simpelt diagram.
Kortfattet: Mens vi kan repræsentere fluorophosphationen (PO3F2-) strukturelt, forstås Na2PO3F selv bedst som en kombination af natriumioner og et netværk af fluorophosphationer i et fast gitter.
Sidste artikelHvad er zirconium og nitrogen lige?
Næste artikelHvor mange flere valenselektroner har natrium brug for at have en fuld?
 Varme artikler
Varme artikler
-
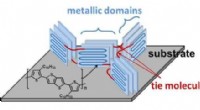 Uvridende plastik til opladning af Internet-of-Things-enhederTil venstre:Forskerne fandt ud af, at deres dopingteknik dannede bindinger (røde) mellem PBTTTs krystallinske dele (blå rektangler). Til højre:De fandt også ud af, at PBTTT var snoet i sin naturlige t
Uvridende plastik til opladning af Internet-of-Things-enhederTil venstre:Forskerne fandt ud af, at deres dopingteknik dannede bindinger (røde) mellem PBTTTs krystallinske dele (blå rektangler). Til højre:De fandt også ud af, at PBTTT var snoet i sin naturlige t -
 En ny krydskobling forenkler syntesen af lægemiddellignende molekylerPhil Baran, PhD, seniorforfatter af undersøgelsen og Darlene Shiley professor i kemi ved TSRI. Kredit:John D. &Catherine T. MacArthur Foundation. Forskere ved The Scripps Research Institute (TSRI)
En ny krydskobling forenkler syntesen af lægemiddellignende molekylerPhil Baran, PhD, seniorforfatter af undersøgelsen og Darlene Shiley professor i kemi ved TSRI. Kredit:John D. &Catherine T. MacArthur Foundation. Forskere ved The Scripps Research Institute (TSRI) -
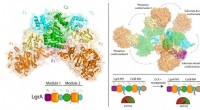 Ny forståelse af antibiotikasynteseKredit:McGill University Forskere ved McGill Universitys medicinske fakultet har gjort vigtige fremskridt med at forstå funktionen af enzymer, der spiller en integreret rolle i produktionen af
Ny forståelse af antibiotikasynteseKredit:McGill University Forskere ved McGill Universitys medicinske fakultet har gjort vigtige fremskridt med at forstå funktionen af enzymer, der spiller en integreret rolle i produktionen af -
 Neutronmicellemålinger giver indsigt i forbedret lægemiddelleveringTyler Cooksey, en kandidatforsker ved University of Houston, bruger ORNLs Bio-SANS-instrument ved High Flux Isotope Reactor til at forstå, hvordan miceller kan forbedres for at skabe mere effektive læ
Neutronmicellemålinger giver indsigt i forbedret lægemiddelleveringTyler Cooksey, en kandidatforsker ved University of Houston, bruger ORNLs Bio-SANS-instrument ved High Flux Isotope Reactor til at forstå, hvordan miceller kan forbedres for at skabe mere effektive læ


