Hvor mange flere valenselektroner har natrium brug for at have en fuld?
Her er hvorfor:
* natriums elektronkonfiguration: Natrium har 11 elektroner. Dens elektronkonfiguration er 2, 8, 1. Dette betyder, at den har en elektron i sin yderste skal (den tredje skal).
* fuld ydre skal: En fuld ydre skal til natrium ville have 8 elektroner.
* octet regel: Atomer har en tendens til at vinde, miste eller dele elektroner for at opnå en fuld ydre skal (8 elektroner, med undtagelse af helium, der har 2).
Natrium opnår en fuld ydre skal ved at miste sin ene valenselektron og blive en positivt ladet ion (Na+). Dette er grunden til, at natrium er meget reaktiv og danner let ioniske bindinger med elementer, der har en tendens til at få elektroner.
Sidste artikelHvad er molekylstrukturen for Na2PO3F?
Næste artikelHvad er CO IT neutral oxid surt eller grundlæggende oxid?
 Varme artikler
Varme artikler
-
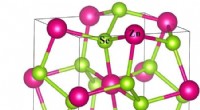 Forskere opdager mekanismer bag termoelektrisk materialeDe pyrit-type krystalstrukturer af ZnSe 2 . Kredit:JIA Tiantian For nylig, en forskergruppe ledet af prof. Zhang Yongsheng fra Institute of Solid State Physics, Hefei Institutes of Physical Scie
Forskere opdager mekanismer bag termoelektrisk materialeDe pyrit-type krystalstrukturer af ZnSe 2 . Kredit:JIA Tiantian For nylig, en forskergruppe ledet af prof. Zhang Yongsheng fra Institute of Solid State Physics, Hefei Institutes of Physical Scie -
 Mod forbedret sårheling:Kemisk syntese af et trefoil faktor peptidUndersøgelser viste, at trefoil-faktor-peptider produceres lokalt for at bekæmpe inflammation og skader i mave-tarmkanalen ved at fremskynde sårheling. Kredit:Universität Wien Den fascinerende fam
Mod forbedret sårheling:Kemisk syntese af et trefoil faktor peptidUndersøgelser viste, at trefoil-faktor-peptider produceres lokalt for at bekæmpe inflammation og skader i mave-tarmkanalen ved at fremskynde sårheling. Kredit:Universität Wien Den fascinerende fam -
 Bestemmelse af, hvad der binder til slimKredit:American Chemical Society Menneskekroppen er fuld af slim. Denne tyktflydende goo er ikke bare en gene, der bliver hostet eller nyset ud - det kan binde sig til medicin, toksiner eller mikr
Bestemmelse af, hvad der binder til slimKredit:American Chemical Society Menneskekroppen er fuld af slim. Denne tyktflydende goo er ikke bare en gene, der bliver hostet eller nyset ud - det kan binde sig til medicin, toksiner eller mikr -
 Kunstige bier fra en trykkoger?Ola Gjønnes Grendal bruger en metode, der fungerer som en trykkoger, til at skabe et materiale, der kan forvandles til kunstige bier. Kredit:Karoline Ravndal Lorentzen, NTNU Hvad hvis vi kunne ska
Kunstige bier fra en trykkoger?Ola Gjønnes Grendal bruger en metode, der fungerer som en trykkoger, til at skabe et materiale, der kan forvandles til kunstige bier. Kredit:Karoline Ravndal Lorentzen, NTNU Hvad hvis vi kunne ska
- Ændrer tiden hastigheden?
- Findes granit og basalt i vulkaner?
- Hvordan er en mest sandsynlig oxidationstilstand relateret til dens valenselektroner?
- Philips Lighting slutter sig til Amsterdams førsteklasses AEX-indeks
- Amazon og Alphabet kunne slutte sig til '$1.000 Stock Club', men er det et tegn på problemer?
- Forskere udvikler en ny inhalationsvaccineplatform med tørt pulver


