Hvilket element kan danne en forbindelse med CAXO4?
* Identificer de kendte dele:
* CA: Calcium, et alkalisk jordmetal (gruppe 2)
* o: Ilt, en ikke-metal (gruppe 16)
* x: Det ukendte element
* Overvej anklagerne:
* Calcium (CA) danner normalt en +2 ion (Ca²⁺).
* Oxygen (O) danner normalt en -2 ion (O²⁻).
* Vi er nødt til at bestemme ladningen på det ukendte element (x) for at afbalancere forbindelsen.
* Forbindelsen er neutral: Den samlede ladning af forbindelsen skal være nul.
Deduktion:
Da CA har en +2 ladning, og hvert ilt har en -2 -ladning, er den samlede ladning fra CA og O allerede afbalanceret:(+2) +4 (-2) =-6.
For at afbalancere den samlede ladning af forbindelsen til nul, skal det ukendte element (x) have en +6 ladning.
Mulige elementer:
* krom (CR): Krom kan danne en +6 oxidationstilstand i forbindelser som kromater (Cro₄²⁻).
Derfor kan en mulig forbindelse være cacro₄, calciumchromat.
Vigtig note: Der kan være andre elementer, der kan danne en forbindelse med CAXO4 under specifikke betingelser, men krom er den mest sandsynlige kandidat i betragtning af de almindelige oxidationstilstande.
Sidste artikelHvad er to processer, der danner forskellige oxider?
Næste artikelHvilket oxid bruges i hvide malinger?
 Varme artikler
Varme artikler
-
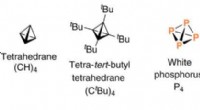 Isolering af en undvigende phosphatetrahedraneOversigt over forbindelser, der er relevante for denne undersøgelse. Kredit: Videnskab fremskridt , doi:10.1126/sciadv.aaz3168 Et forskerhold i Institut for Kemi ved Massachusetts Institute of Te
Isolering af en undvigende phosphatetrahedraneOversigt over forbindelser, der er relevante for denne undersøgelse. Kredit: Videnskab fremskridt , doi:10.1126/sciadv.aaz3168 Et forskerhold i Institut for Kemi ved Massachusetts Institute of Te -
 Team rapporterer teknologi, der muliggør præcisionsantibiotikaBoston College -forskere kemisk modificerede en fagvisning for at udvikle en ny tilgang til at finde specifikke bakteriestammer og målrette dem med antibiotika. Kredit: Journal of the American Chemica
Team rapporterer teknologi, der muliggør præcisionsantibiotikaBoston College -forskere kemisk modificerede en fagvisning for at udvikle en ny tilgang til at finde specifikke bakteriestammer og målrette dem med antibiotika. Kredit: Journal of the American Chemica -
 Kemikere ID mulig afhængighedsfri smertelindringKredit:CC0 Public Domain Anslået 1,7 millioner amerikanere lider af stofmisbrugslidelser relateret til opioidbrug til smertelindring, ifølge National Institute on Drug Abuse. Dette forårsager en ø
Kemikere ID mulig afhængighedsfri smertelindringKredit:CC0 Public Domain Anslået 1,7 millioner amerikanere lider af stofmisbrugslidelser relateret til opioidbrug til smertelindring, ifølge National Institute on Drug Abuse. Dette forårsager en ø -
 Æteriske oliekomponenter kan testes som lægemiddelkandidaterKredit:CC0 Public Domain Et forskerhold ved VIB-KU Leuven Center for Mikrobiologi og KU Leuven Biologisk Institut viste, at i modsætning til almindelig tro, de fleste komponenter i æteriske olier
Æteriske oliekomponenter kan testes som lægemiddelkandidaterKredit:CC0 Public Domain Et forskerhold ved VIB-KU Leuven Center for Mikrobiologi og KU Leuven Biologisk Institut viste, at i modsætning til almindelig tro, de fleste komponenter i æteriske olier
- At gøre byer køligere er en no brainer – så hvorfor gør vi så lidt ved det?
- En organisk transistor baner vejen for nye generationer af neuro-inspirerede computere
- USA skal overhale Saudi som råolieproducent:IEA
- Hvordan Kindle Unlimited sammenlignes med Scribd, Oyster
- Hvad er KEQ for reaktionen N2 3H2 2NH3 Hvis ligevægtskoncentrationer er NH3 2 m 3 og H2 1 m?
- Australien har en stærk hånd til at tackle hasardspilskader. Vil det gå all in eller foldes?


